ХИМИЧКА
Опыты в домашней лаборатории

Этот раздел был создан исключительно для вашей безопасности, поэтому прочтите его, пожалуйста. Все опыты полностью безопасны, если у вас есть достаточные химические знания. Так что перед работой обязательно проанализируйте описание эксперимента, просмотрите примечания про технику исполнения и правила безопасности. В случае необходимости обратитесь за консультацией к учителю или почитайте дополнительную литературу. Можете быть уверены, что при точном выполнении приведённых ниже советов вы не получите травм или отравлений при работе с химическими веществами. Итак, вот основные и самые важные правила:
1) НИКОГДА не пробуйте на вкус и не нюхайте химические вещества!
2) При работе с открытым пламенем соблюдайте правила противопожарной безопасности.
3) Если вы хотите добавить спирт в спиртовку, то её обязательно необходимо потушить перед доливанием.
4) Если вам необходимо сделать раствор кислоты, то необходимо лить кислоту в воду, а не наоборот. Для того чтоб запомнить это, существует простенький стишок:
Сначала вода, потом кислота,
иначе случится большая беда!
5) После проведения ЛЮБОГО эксперимента тщательно вымойте руки.
6) Никогда не кушайте во время проведения эксперимента.
7) Никогда не кладите еду на стол, на котором проводится опыт или на котором находятся реактивы.
8) При проведении опытов берите только те количества вещества и соблюдайте те пропорции, которые указаны в описании опыта.
9) Если необходимо понюхать какое-либо вещество, то не подносите его к носу, а совершите несколько движений рукой от вещества к носу и понюхайте воздух.
10) После проведения эксперимента обязательно вытрите стол, на котором он проводился.
11) Если необходимо нагреть что-либо в стеклянной химической посуде, то сначала слегка нагрейте эту ёмкость проводя ей над пламенем спиртовки.
Несколько полезных советов.
Вот несколько советов, которые могут вам понадобиться для проведения многих опытов:
1) Во время работы с различными солями желательно надеть одноразовые резиновые перчатки, т. к. кожа имеет свойство впитывать вещества, попавшие на неё.
2) Наиболее токсичными являются соли следующих металлов: Hg, Pb, Cd, Со, Ni, Zn, Ва, Sb, Sr, Сr; менее токсичны соли Си, Fe, Аl, Аg; и наименее токсичны соли Са, К, Na и Мg. Но работать необходимо осторожно со всеми веществами.
3) Я советую завести специальное полотенце (предпочтительно вафельное) для вытирания вымытой химической посуды.
4) Если после кипячения раствора на стенках химической посуды остался несмываемый налёт, то его можно удалить, ополоснув ёмкость раствором соляной кислоты.
5) Если для проведения эксперимента вам необходим пробиркодержатель, а у вас его нет, то его можно сделать из обычной деревянной (не пластмассовой!) прищепки.
Если вы по каким-то причинам не можете заказать специальные химические реактивы, попробуйте найти их среди товаров народного потребления (на примере Москвы):
Азотная кислота — на Митинском радиорынке.
Алюминий — на строительном рынке, в пунктах приема металлолома Аммиак водный (нашатырный спирт) — в аптеке.
Ацетат свинца — в аптеке.
Ацетон (диметилкетон) — в хозмаге среди растворителей.
Бензин — в хозмаге среди растворителей, на автозаправочной станции.
Борная кислота — в аптеке.
Висмут — в припоях, особенно легкоплавких.
Гексаметилентетрамин (уротропин, сухой спирт) — в туристическом магазине.
Гидрокарбонат натрия (сода) — в продовольственном магазине.
Гидроксид калия (КОН) — на Митинском радиорынке.
Гидроксид кальция (гашеная известь[95]) — на строительном рынке, в крупном хозмаге.
Гидроксид натрия (едкий натр) — в хозмаге продается как средство для прочистки труб "Крот".
Гидропирит — в аптеке.
Глицерин[96] — на радиорынке, в магазинах радиодеталей.
Глюкоза — в аптеке.
Графит — в простых карандашах, на радиорынке.
Диоксид кремния (кварцевый песок) — на строительном рынке.
Дистиллированная вода — в аптеке.
Дихлорэтан — в хозмаге (клей для оргстекла).
Дихромат калия К2Сr2O7 — используется как оранжевая краска, продаётся в виде порошка под названием "хромпик".
Йод — в аптеке.
Желатин — в продовольственном магазине.
Золото — в ювелирных ларьках[97], в магазинах сырья для ювелиров.
Карбамид (мочевина) — в хозмаге, в отделе удобрений.
Карбонат кальция (мел) — в канцтоварах, на строительном рынке.
Карбонат натрия (стиральная сода, кальцинированная сода) — в хозмаге. Кевлар (нить) — в рыболовном магазине.
Крахмал — в продовольственном магазине.
Интерферон — в аптеке.
Изопропанол (баллончик для очистки дисплеев и контактов) — в крупных компьютерных и радиомагазинах.
Лимонная кислота — в продовольственном магазине.
Марганцевокислый калий KMnO4 — марганцовка, продаётся в аптеках.
Медь — в пунктах приема металлолома, в электротехнических изделиях Нафталин — в хозмаге (средство от моли).
Нитрат аммония (аммиачная селитра) — в хозмаге, среди удобрений.
Нитрат калия KNO3 (калиевая селитра) и нитрат натрия NaNO3 (натриевая селитра) — удобрения, продающиеся в с/х магазинах.
Нитрат кальция (кальциевая селитра) — в хозмаге, среди удобрений.
Нитрат серебра (ляписный карандаш) — в аптеке.
Оксид кальция (негашеная известь) — в хозмаге, на строительном рынке.
Оксид магния (жженая магнезия) — в аптеке.
Оксид хрома(III) Сr2O3 — очень устойчивая зелёная краска, называется "хромовый зелёный". Продаётся в хоз. магазинах.
Олово — в припоях.
Ортофосфорная кислота — на Митинском радиорынке.
Парафин — в хозмаге, в свечках.
Перманганат калия (марганцовка) — в аптеке.
Пероксид водорода (перекись водорода) — в аптеке.
Персульфат аммония — на радиорынке, в магазинах для любителей традиционной (нецифровой) фотографии.
Порох — в охотничьих магазинах, петардах и фейерверках.
Резорцин — в аптеке.
Сахароза (сахар) — в продовольственном магазине.
Сера S — продаётся в виде порошка и серных шашек. Порошок применяется для опрыскивания растений, а шашки для выкуривания насекомых-вредителей.
Серебро — в ювелирных ларьках, в магазинах сырья для ювелиров.
Свинец[98] — в пунктах приема металлолома, в автомобильных аккумуляторах
Серная кислота — в автомагазине.
Силикат натрия Na2SiO3 (метасиликат) — в хозмаге, на строительном рынке — это силикатный клей, продающийся в магазинах канцелярских принадлежностей. Часто его продают на разлив под названием "жидкое стекло".
Слюда — на Митинском радиорынке.
Соляная кислота — на Митинском радиорынке.
Стеарат натрия (хозяйственное мыло) — в хозмаге.
Сульфат железа FeSO4*7Н2О (железный купорос) — в хозмаге, с/х магазинах.
Сульфат меди CuSO4*5Н2O (медный купорос) — в хозмаге, среди средств по борьбе с плесенью.
Сульфит натрия — в магазинах для любителей традиционной (нецифровой) фотографии — проявитель.
Тетраборнокислый натрий (бура) Nа2В4O7*10Н2O — это вещество используется для пайки. Купить его можно на радиорынке.
Тимол — в аптеке.
Ферроцианид калия (желтая кровяная соль) — в магазинах для любителей традиционной (нецифровой) фотографии.
Фоторезист — на радиорынке, в магазинах радиодеталей.
Фторопласт — на Митинском радиорынке.
Уайт-спирит — в хозмаге.
Уголь активированный — в аптеке.
Уголь древесный — в хозмаге.
Уголь каменный — на строительном рынке.
Уксусная кислота — в продовольственном магазине.
Фенолфталеин — входит в состав некоторых слабительных препаратов, таких, как пурген и фенолфталеин. Продаётся в аптеках.
Формиат натрия — в хозмаге или на строительном рынке — это жидкость для отопительных систем.
Хлорид аммония — на радиорынке.
Хлорид-гипохлорит кальция (хлорка) — в хозмаге.
Хлорид железа (хлорное железо) — на радиорынке, в радиомагазине.
Хлорид кальция — в аптеке.
Хлорид натрия (поваренная соль) — в продовольственном магазине.
Целлюлоза (вата) — в аптеке.
Цинк — в батарейках (особенно советских).
Этиленгликоль — в автомагазине — это антифриз[99].
Этиловый спирт С2Н5OН — лучше всего покупать его в аптеках.
Лабораторная посуда
1. Пробирка химическая используется для проведения большинства простейших опытов и как деталь собираемых приборов.
2. 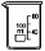 Стакан с носиком служит для хранения жидких и твердых веществ, а также для проведения простейших химических операций (растворение, нагревание).
Стакан с носиком служит для хранения жидких и твердых веществ, а также для проведения простейших химических операций (растворение, нагревание).
3.  Колба коническая используется для хранения жидких и твердых веществ, а также для проведения различных химических операций.
Колба коническая используется для хранения жидких и твердых веществ, а также для проведения различных химических операций.
4. Колба круглодонная служит для проведения разнообразных химических операций при нагревании.
5. Колба с отростком предназначена для перегонки и разделения жидкостей при нагревании.
6. Колба плоскодонная служит для проведения химических операций, а также для хранения жидких и твердых веществ.
7.  Мерная посуда: цилиндр (рис), стакан и пробирка — используют для измерения объема жидкостей.
Мерная посуда: цилиндр (рис), стакан и пробирка — используют для измерения объема жидкостей.
8. Воронка конусообразная служит для переливания жидкостей и фильтрования.
Воронка конусообразная служит для переливания жидкостей и фильтрования.
9. Стеклянная палочка предназначена для размешивания веществ в химической посуде. Для предохранения посуды от случайного растрескивания при размешивании веществ на конец стеклянной палочки надевают кусочек резиновой трубки.
Стеклянная палочка предназначена для размешивания веществ в химической посуде. Для предохранения посуды от случайного растрескивания при размешивании веществ на конец стеклянной палочки надевают кусочек резиновой трубки.
10.  Ложка фарфоровая (1), шпатель (2) служат для взятия твердых и сыпучих веществ. Ложка-дозатор (3) предназначена для взятия определенной порции вещества.
Ложка фарфоровая (1), шпатель (2) служат для взятия твердых и сыпучих веществ. Ложка-дозатор (3) предназначена для взятия определенной порции вещества.
11.  Чашка фарфоровая применяется для выпаривания жидкостей.
Чашка фарфоровая применяется для выпаривания жидкостей.
12.  Тигель фарфоровый предназначен для нагревания и прокаливания твердых веществ при высокой температуре.
Тигель фарфоровый предназначен для нагревания и прокаливания твердых веществ при высокой температуре.
13.  Треугольник фарфоровый используется для размещения в нем тигля. Треугольник помещают на кольцо штатива.
Треугольник фарфоровый используется для размещения в нем тигля. Треугольник помещают на кольцо штатива.
14.  Ступка с пестиком служат для размельчения и растирания твердых веществ.
Ступка с пестиком служат для размельчения и растирания твердых веществ.
15.  Штатив для пробирок, служит для размещения в нем пробирок.
Штатив для пробирок, служит для размещения в нем пробирок.
16.  Зажим пробирочный служит для закрепления пробирки, если вещество в пробирке требуется нагреть в пламени.
Зажим пробирочный служит для закрепления пробирки, если вещество в пробирке требуется нагреть в пламени.
17.  Зажим пружинный используют для зажимания резиновых трубок при монтаже различных приборов.
Зажим пружинный используют для зажимания резиновых трубок при монтаже различных приборов.
18.  Промывалка служит для промывания осадков дистиллированной водой, для смывания осадков с фильтров и стенок сосудов. Ее используют также для хранения небольших количеств дистиллированной воды.
Промывалка служит для промывания осадков дистиллированной водой, для смывания осадков с фильтров и стенок сосудов. Ее используют также для хранения небольших количеств дистиллированной воды.
19.  Воронка делительная предназначена для разделения несмешивающихся жидкостей, имеющих разную плотность.
Воронка делительная предназначена для разделения несмешивающихся жидкостей, имеющих разную плотность.
20.  Склянка с пипеткой служит для хранения растворов реактивов при работе с малыми количествами веществ.
Склянка с пипеткой служит для хранения растворов реактивов при работе с малыми количествами веществ.
21. Пластина для капельного анализа (керамическая или стеклянная) используется при выполнении опытов с очень малыми количествами веществ в объеме 1–2 капель.
22.  Прокладка керамическая огнезащитная используется при нагревании веществ в стеклянной посуде. Прокладку размещают на кольце металлического штатива.
Прокладка керамическая огнезащитная используется при нагревании веществ в стеклянной посуде. Прокладку размещают на кольце металлического штатива.
(В.Н.Верховский "Техника Химического Эксперимента")
Приборы периодического действия
Вот простейший из вышеуказанных приборов, состоящий из банки с жидкостью и пробирки с веществом. Пробирка держится в пробке, вставленной в горло склянки, и может быть погружена в жидкость. На конце пробирки сделано отверстие таких размеров, чтобы через него не могли проскочить помещенные в пробирку кусочки твердого вещества. На дно пробирки кладут несколько кусков стекла. Через отверстие в пробирку входит налитая в банку жидкость. Газ выходит через присоединенную к пробирке газоотводную трубку. Чем большее сопротивление должен преодолеть газ, тем глубже должна быть погружена в жидкость пробирка. Отверстие в дне пробирки можно сделать при помощи напильника, точильного камня или карборундового бруска, спилив самую нижнюю часть дна (держать напильник перпендикулярно к оси пробирки). Но лучше «продуть» отверстие, нагрев дно пробирки на остром пламени паяльной горелки или оттянуть конец пробирки и обрезать его. В последнем случае вместо пробирки можно воспользоваться трубкой подходящего диаметра.

Пробка, вставленная в пробирку, должна хорошо держать. Пробка же, в которой укреплена пробирка, наоборот, не должна прилегать слишком плотно к горлышку банки, чтобы жидкость в банке имела сообщение с атмосферой. Можно прорезать в пробке сбоку продольную щель. Если пробирка плохо держится в отверстии пробки и съезжает вниз, ее можно укреплять при помощи небольшого клина из спички и т. п. Вместо пробирки можно воспользоваться сеткой из такого материала, на который не действует жидкость, служащая для получения газа. Например, при получении оксида углерода СO2 взаимодействием мрамора с разбавленной соляной кислотой берут медную сетку, делают из нее мешочек или корзиночку (рис. 2), которую подвешивают на крючке из проволоки или стеклянной палочки. Крючок можно передвигать в пробке, вставленной в банку с жидкостью. Газ выходит через газоотводную трубку, находящуюся в той же пробке.

Такие приборы позволяют регулировать ток газа. Это имеет большое преимущество, особенно если требуется ровная струя газа или во время опыта необходимо изменять силу тока газа, а также если газ бывает нужен в определенные промежутки времени. Пока газ не нужен, реакция не идет и вещества не расходуются без надобности. Простейший небольшой прибор такого рода отличается от данного на рисунке 1 прибора тем, что снабжен краном или зажимом на каучуке. При закрывании крана образующийся газ вытесняет жидкость из пробирки, и реакция прекращается. Таким образом, для прекращения реакции нет необходимости поднимать пробирку. (В пробке должен быть вырез 1.) Чтобы прибор хорошо действовал, конец пробирки с твердым веществом лучше оттянуть подлиннее. Кусочки вещества не должны быть слишком мелкие, чтобы они не проваливались глубоко, в оттянутый конец пробирки, иначе после закрывания крана жидкость будет касаться твердого вещества и газ будет непрерывно выходить из пробирки. Если пробирка хорошо оттянута и куски твердого вещества достаточно крупные, то между твердым веществом и жидкостью будет оставаться слой газа, который и будет препятствовать их соприкосновению, пока прибор не работает. В нижнюю часть пробирки можно положить куски стекла для лучшего разделения твердого вещества от жидкости в то время, когда кран закрыт. Обычно после закрывания крана некоторое количество газа выходит наружу (пробулькивает), пока идет реакция между твердым веществом и не успевшей стечь с него жидкостью. Если прибор не используют долгое время, пробирку с твердым веществом можно поднять, как в приборе, изображенном на рисунке 4.

Нижнее отверстие пробирки с твердым веществом должно быть достаточно велико (2–3 мм), так как через него во время действия прибора проходят два тока жидкости: вверх — реагирующая жидкость, вниз — более тяжелый раствор, содержащий продукты реакции между жидкостью и твердым веществом (обычно раствор соли). На рисунке 4 изображен приборчик для получения газов. В одно из колен U-образной трубки в корзиночке из медной сетки помещены кусочки твердого вещества (цинк, мрамор и др.). В трубку наливают разбавленную кислоту. Когда зажим закрыт, прибор не действует.
В качестве автоматического прибора можно использовать склянку Тищенко. Кусочки твердого вещества должны быть в этом случае достаточно мелки, чтобы они проходили в узкое горлышко склянки. Для наполнения кислотой склянку наклоняют почти горизонтально и кислоту наливают через воронку с узким, оттянутым и изогнутым концом, который входил бы в боковой отросток склянки. Зажим при этом должен быть закрыт. Можно также сначала налить в склянку через горлышко кислоту, затем присоединить к отростку склянки каучук, через который ртом высасывать воздух, пока кислота не перейдет в левую половину склянки, после чего зажать каучук (пальцами или зажимом), всыпать через горлышко цинк, вставить в склянку пробку и снять каучук с отростка. Склянку Тищенко следует выбрать с возможно малым отверстием в перегородке. Большое преимущество такого прибора — устойчивость и простота обращения при работе. Для лабораторных опытов учащихся очень удобны небольшие автоматические приборы, имеющиеся в продаже, а также самодельные — из большой пробирки или широкой стеклянной трубки (рис. 5).

Твердое вещество (цинк, мрамор и пр.) помещают в этих приборах на резиновый кружок с вырезами (рис. 5), надетый на трубку воронки и свободно входящий в пробирку (кусочки твердого вещества не должны проваливаться в вырезы и в зазор между кружком и стенками реакционного сосуда). Жидкость наливают через воронку при открытом (винтовом) зажиме в таком количестве, чтобы слой ее над твердым веществом был высотой 2–3 см. При перекрытии резиновой газоотводной трубки зажимом жидкость давлением газа вытесняется в воронку, стекает с твердого вещества через вырезы в резиновом кружке, и реакция прекращается. Для возобновления ее достаточно открыть зажим. Все эти приборы употребляют главным образом для получения небольших количеств газов при лабораторных опытах учащихся. Чтобы получать большие количества газа, который выходил бы из прибора сильной струей, пользуются общеизвестными приборами Сен-Клер-Девиля и Киппа. Прибор Сен-Клер-Девиля изображен на рисунке 6.
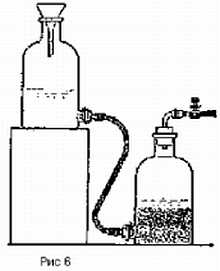
Он состоит из двух склянок с тубулусами (в 1–4 и более литров), соединенных каучуковой трубкой. В одной склянке находится твердое вещество, в другую наливают жидкость. Склянку с жидкостью помещают выше склянки с твердым веществом, но жидкость попадает к твердому веществу только в том случае, если открыт кран или зажим на газоотводной трубке и жидкость может вытеснить из склянки с твердым веществом находящийся в ней газ (при начале работы — воздух). После закрывания крана или зажима образующийся газ вытесняет жидкость обратно в стоящую выше склянку, и реакция прекращается. Чем выше поставлена склянка с жидкостью относительно склянки с твердым веществом, тем сильнее может быть струя газа и тем большее сопротивление она может преодолеть. Возможность получать значительное давление газа составляет большое преимущество прибора Сен-Клер-Девиля по сравнению с большинством других приборов для получения газов при взаимодействии жидкости твердым веществом. При устройстве прибора Сен-Клер-Девиля на дно склянки, предназначаемой для твердого вещества, насыпают сначала слой битого стекла, фарфора, стеклянных бус, крупного гравия, черепков от глиняной посуды и т. п., а затем уже насыпают твердое вещество, участвующее в реакции получения газа.
Насыпание индиферентного вещества имеет еще то преимущество, что после окончания работы, когда главная масса жидкости вытеснена в верхнюю склянку, часть нижней склянки, заполненная стеклом и т. п., представляет собой резервуар, наполняющийся газом, который продолжает выделяться вследствие действия на твердое вещество, еще не успевшей стечь с него, части жидкости. Чем больше слой индиферентного вещества, тем меньше газа может выйти из прибора через соединительную трубку и через слой жидкости в верхней склянке. Газ выходит обыкновенно большими пузырями, что сопровождается сильным бульканьем, отвлекающим внимание учащихся от опыта. Чтобы _ избежать этого, следует не сразу закрывать кран, а несколько раз приоткрывать его, чтобы выпустить избыток газа, если позволяют условия опыта. При прохождении пузырей газа через слой жидкости в верхней склянке из нее могут вылетать брызги жидкости, поэтому в склянку с жидкостью вставляют небольшую воронку, которая служит также и для наливания свежей жидкости. Пробки к нижним тубулусам склянок для аппарата Сен-Клер-Девиля должны быть обязательно резиновые, их необходимо привязывать. Длина каучуковой трубки, соединяющей склянки большого объема, 50–60 см, наружный диаметр около 1 см, а толщина стенок 1,5–2 мм. Стеклянные трубки, вставленные в нижние пробки и служащие для надевания соединяющего склянки каучука, должны быть хорошо оплавлены, концы их могут выставляться из пробок не более чем на 3–4 см. Соединительную резиновую трубку следует к ним привязать, для чего на концах стеклянных трубок желательно сделать небольшие перетяжки, как на соединительных и переходных трубках. Для регулирования выхода газа применяют стеклянный кран, согнув одну из трубок его под прямым углом, но можно удовольствоваться и винтовым зажимом. Пока прибор не нужен, склянку с кислотой ставят ниже склянки с твердым веществом: прибор в таком положении может храниться долгое время.

Для удобства пользования и хранения полезно сделать для прибора Сен-Клер-Девиля деревянный ящик, открытый с одной стороны. При хранении прибора можно склянку с жидкостью ставить внутрь ящика, а с твердым веществом — наверх. В таком виде прибор занимает мало места. При снаряжении прибора твердого вещества обыкновенно накладывают побольше, чтобы не приходилось очень часто переснаряжать его (но следует иметь в виду, что, чем больше твердого вещества, тем больше будет выделяться газа после закрывания крана). Жидкости наливают не более половины склянки. Если образующийся газ горюч, то каждый раз после добавления в прибор твердого вещества вытесняют из прибора весь воздух, чтобы не образовалась взрывчатая смесь. При отсутствии склянок с тубулусами можно сделать прибор Сен-Клер-Девиля из обычных склянок (бутылок) достаточного объема (рис. 8).

В таком приборе жидкость переливается в реакционную склянку с помощью сифонной трубки и вытесняется в верхний сосуд давлением газа при перекрывании! газоотводной трубки зажимом.
Аппарат Киппа
Широко используется аппарат Киппа(рис. 10 и 11)


Твердое вещество помещают в средней части сосуда, отделенной от нижней перетяжкой, благодаря чему оно не соприкасается с остающейся на дне прибора жидкостью, когда прибор отключен. Нижняя часть сосуда в приборе Киппа играет ту же роль, что и пространство между кусками индиферентного вещества в приборе Сен-Клер-Девиля. Воронка вставлена в прибор на шлифе, газоотводная трубка с краном или зажимом — на пробке, лучше каучуковой. Нижний тубулус служит для выливания отработавшей жидкости. Твердое вещество вносят через тубулус. Чтобы твердое вещество не проваливалось вниз, отверстие между средним шаром и нижней частью прибора закрывают кружком из твердой резиновой пластины. В этом кружке прорезают широкое отверстие посередине для трубки воронки прибора и несколько небольших отверстий, через которые свободно могла бы проходить жидкость. Иногда приборы Киппа делают с соответствующим приспособлением из стекла в виде вставленной в перетяжку сосуда широкой трубки с отверстиями (рис. 11). Эта трубка, вставленная в перетяжку сосуда, должна иметь достаточно большие отверстия, расположенные не слишком высоко. В противном случае кислота не успевает стекать в нижнюю часть прибора или не имеет возможности стечь, и реакция продолжается еще долгое время после закрытия крана. Выделяющийся газ при этом проходит в нижнюю часть прибора и через трубку воронки пробулькивает в верхний шар большими пузырями, вызывая напрасный расход реактивов и разбрызгивание кислоты из отверстия (рекомендуется поэтому всегда держать в верхнем отверстии шара небольшую воронку). Если вставная трубка имеет очень маленькие или слишком низко расположенные отверстия, то лучше удалить ее совсем, заменив резиновым или пластмассовым кружком, или вставить в отверстие перетяжки свернутую в трубку пластмассовую сетку, из которой обычно делают сейчас прокладки для пластинок свинцовых аккумуляторов. Прежде чем снаряжать прибор, следует смазать вазелиновой мазью все пришлифованные части.
Нижнюю и верхнюю (с краном) пробки необходимо привязать медной проволокой. Очень удобны для этого тонкие электрические многожильные провода в пластмассовой изоляции. Если пробки притертые, то сначала обматывают в 3–4 витка провод у толстого ранта тубулуса, наложив провод так, чтобы остались два одинаковых длинных конца. Эти концы скручивают, перекидывают скрученную часть на головку пробки, охватывая ее проводом с двух сторон, снова скручивают концы и перекидывают провод к ранту тубулуса, охватывая горло его с двух сторон, и опять скручивают концы. Во избежание потери времени на развязывание и привязывание пробки, что приходится делать при каждой перезарядке, удобнее сделать для нее запор, изображенный на рисунке 12.

Для устройства этого запора горло тубулуса обвивают проволокой, на которой делают две петли — одна против другой. В одну петлю вставляют конец длинной медной или лучше алюминиевой пластинки и огибают ее вокруг проволоки так, чтобы полоска могла откидываться на петле, как на шарнире. Пластинка должна быть вырезана и выгнута так, как показано на рисунке, чтобы она охватывала пробку с обеих сторон двумя боковыми отростками, оставленными посередине пластинки. Свободный конец пластинки выгибают в виде крючка, который может быть притянут ко второму сделанному на проволоке кольцу при помощи колечка, отрезанного от каучуковой трубки. Проволоку и пластинку лучше всего взять алюминиевые. Тогда приспособление будет служить много лет. Придется только иногда менять резиновое колечко.
Резание стеклянных трубок
Чтобы отрезать кусок трубки определенной длины, нужно сначала отметить место надреза, взять трубку в левую руку, зажать ее между указательным и большим пальцами и ножом для резки стекла или трехгранным напильником сделать царапину. После этого, держа трубку обеими руками так, чтобы царапина приходилась между ними, слегка согнуть трубку со стороны, противоположной царапине. На месте царапины трубка обычно ломается. Если при небольшом усилии этого не произойдет, царапину несколько расширить и растягивание повторить. После того как трубка отрезана, концы ее следует оплавить. Для этого внести конец трубки наклонно в несветящееся пламя горелки, все время поворачивая трубку вокруг оси до тех пор, пока конец не накалится. Затем вынуть трубку из пламени и положить для остывания на сетку с асбестом (но не на стол!)
Сгибание стеклянных трубок
Надеть на горелку насадку («ласточкин хвост»), зажечь горелку и равномерно нагреть место сгиба (см. рисунок), спокойно вращая трубку вокруг оси. Когда трубка размягчается, вынуть ее из пламени и плавно согнуть. Правильность сгиба зависит от равномерности нагревания и плавности сгибания. При быстром сгибании трубка будет иметь на сгибе впадину сверху или выемку снизу, что недопустимо.

Правильное и неправильное пользование пробками и трубками:
1 — резание трубки; 2 — правильно согнутая трубка; 3 и 4 — неправильно согнутые трубки; 5 — нагревание трубки в пламени "ласточкиного хвоста"; 6 — трубка, согнутая под прямым углом; 7 — вытягивание трубки.
Вытягивание стеклянных трубок
Довольно часто требуется оттянуть трубку или же вытянуть капилляр. Для этого трубку надо нагреть на протяжении 4–5 см в пламени горелки, все время вращая трубку вокруг оси. После размягчения оттянуть ее до нужного диаметра. Если нужно получить капилляр (очень тонкую трубку с маленьким диаметром), то нагретую до размягчения трубку вынимают из пламени и быстро, но плавно растягивают обеими руками в оба конца.
Подбор пробок
В лаборатории употребляют три сорта пробок: корковые, резиновые и стеклянные. Выбирать корковую пробку следует такого размера, чтобы диаметр ее был немного больше внутреннего диаметра горла сосуда. Затем пробку надо вложить в пробочный пресс и поворачивая, обжимать до тех пор, пока она не станет эластичной и будет плотно входить в горло сосуда. Держа левой рукой горло сосуда у отверстия правой осторожно вставляют пробку в горло, вращая и как бы ввинчивая ее. Пробка должна плотно входить в отверстие.
Сверление пробок
Чтобы просверлить в пробке отверстие, надо сделать на суженной части обжатой пробки отметку той стеклянной трубкой, для которой делается отверстие. Затем подобрать пробочное сверло (рис.) несколько меньшего диаметра, чем наружный диаметр отметки. Сверлить пробку в горизонтальном положении, держа ее в левой руке, а сверло — в правой. Сверлить лучше всего следующим образом: слегка надавливая правой рукой на сверло, делать полуобороты сверлом вправо и влево. Когда сверло войдет в пробку почти до самого края, положить ее на дощечку или на другую пробку и тогда уже осторожно сделать окончательный прорез. Если его делать на весу, то, как правило, края прореза будут рваные. По окончании сверления вытолкнуть шомполом пробковый цилиндрик из сверла. Диаметр сверла при сверлении каучуковых пробок подбирать равным или немного большим вставляемой трубки. В качестве смазывающих веществ, облегчающих сверление резиновых пробок, обычно употребляют вазелиновое масло, глицерин или раствор щелочи. Для подгонки трубок к отверстию корковой пробки иногда делают расточку отверстия круглым напильником. Когда отверстие в пробке готово, смочить кончик отрезанной стеклянной трубки водой и вставить ее в пробку, все время держа трубку правой рукой на расстоянии 2–3 см от пробки и как бы ввинчивая ее. Держать пробку и стеклянную трубку так, чтобы руки были близко одна к другой. От частого употребления сверла тупятся. Тупое сверло рвет пробку, а не режет ее. Чтобы наточить сверло, применяют специальные ножи для точки сверл. Сверло надевают на коническую часть точила, нож прижимают к сверлу. При поворачивании ножа сверло, неподвижно зажатое в левой руке, точится довольно хорошо и быстро.

Сверление пробок:
1 — набор сверл для пробок; 2 — точка сверла; 3 — машинка для сверления пробок; 4 — сверление пробки; 5 — пробкомялка (жом) для пробок
• Никелирование металлических предметов
Металлические изделия и предметы очищают от грязи, обезжиривают раствором соды, промывают в воде, на несколько секунд опускают в 50 %-ный раствор азот ной кислоты и повторно промывают дистиллированной водой. Подготовленное изделие выдерживают 30–50 минут в горячем растворе, содержащем на 1 л воды 280 г гептагидрата сульфата никеля и 100 мл концентрированной соляной кислоты. После получения никелевого покрытия (оно получается плотным и блестящим) изделие промывают водой и полируют суконкой.
• Кристаллы меди
Все умеют выращивать кристаллы различных солей. А вот кристаллы меди не всякий сумеет вырастить. Для этого необычного опыта понадобиться: CuSO4, поваренная соль, кусок жести и стакан (можно обыкновенный). Из куска жести вы режьте круг, чтобы он свободно входил в стакан. В стакан насыпьте порошок сульфата меди(медного купороса) слоем в 5 мм и засыпьте этот слой солью.
ВНИМАНИЕ! Слои не перемешивать. Закройте слои кружком из фильтровальной бумаги и накройте кружком из жести. В стакан налейте раствор соли.

Через две недели вырастут довольно крупные кристаллы меди.
Чтобы они хорошо сохранились поместите их в пробирку с раствором серной кислоты.
• Горение металлов
Горение металлов в кислороде, хлоре широко известно. Менее знакомо горение металлов в парах серы. В штатив укрепляют вертикально большую пробирку, наполненную на одну треть серой, и нагревают до кипения серы. Затем в пробирку опускают пучок тонкой медной проволоки (можно предварительно нагреть) и наблюдают бурную реакцию.
• Золотой дождь

Существует множество веществ с сильной температурной зависимостью растворимости. Именно на этом явлении и основан данный опыт. Для проведения этого опыта необходимо взвесить равные количества ацетата свинца(II) и йодида калия. Далее готовят два раствора. В два химических стакана наливают по 50 мл дистиллированной воды. В один добавляют 1 мл столового уксуса (или ~0,2 мл концентрированной уксусной кислоты) и растворяют ацетат свинца. Кислота добавляется для того, чтобы подавить гидролиз ионов РЬ2+. Во втором растворяют Kl. Затем оба раствора сливают в колбу из огнеупорного стекла объёмом 150 мл. При этом происходит реакция двойного обмена между ацетатом свинца и йодидом калия:
РЬ(СН3СОО)2 + 2KI => 2КСН3СОО + РbI2
После смешивания растворов выпадает жёлтый осадок йодида свинца(II). Смеси растворов в колбе необходимо дать отстояться, чтобы осадок осел полностью. После этого с осадка осторожно сливают жидкость и вместо неё доливают 100 мл дистиллированной воды. Теперь раствор необходимо нагреть до кипения и кипятить в течении 2–3 мин. Осадок должен раствориться полностью. Если всё было сделано правильно, то после охлаждения раствора выпадет множество золотистых кристалликов, которые при встряхивании колбы будут парить в толще воды. Размер кристалликов очень сильно зависит от скорости охлаждения: чем медленнее охлаждать, тем более крупными и красивыми будут кристаллики. Для большей их прочности перед кипячением в раствор добавляют немного глицерина (~0,5 мл на 100 мл раствора).
• Затвердевание жидкости
В химический стакан наливают 20–50 мл силикатного клея (силикат натрия) и добавляют 2–3 мл раствора соляной кислоты (1:1) и тут же перемешивают стеклянной палочкой. Через 30–40 секунд жидкость загустеет и ее уже нельзя вылить из стакана.
• Неорганический сад
Другой, но не менее интересный опыт с силикатом натрия. Готовят горячий (около 60 °C) насыщенный раствор силиката натрия в 100 г воды. Полученный раствор медленно охлаждают до комнатной температуры, при этом образуется вязкая масса, напоминающая по консистенции силикатный клей. Затем берут несколько кристаллов различных окрашенных солей, например, меди, кобальта и никеля. Кристаллы осторожно помещают на дно стакана и оставляют на ночь. Утром можно полюбоваться на "неорганический сад", который вырастет из "семян" — кристаллов.

В методическом отношении, опыт интересен тем, что показывает один из вариантов (хотя и не самый распространенный) образования в природе силикатов, показывает явление осмоса (хотя в школе его не изучают) и еще раз доказывает, что химия не скучная наука.
Уравнение реакции в случае с медным купоросом:
CuSO4 + Na2SiO3 = CuSiO3 + Na2SO4
• "Заживление раны"
Этот опыт демонстрируется в различных вариантах. Перед вами один из них. Кожу руки обильно смачивают "йодом" (слабый раствор хлорного железа), якобы для дезинфекции. После этого набирают в тонкую трубочку раствор роданида калия и проводят концом этой трубочки по смоченному месту (для усиления эффекта опыта можно использовать тупой нож). На руке появляется "кровоточащая рана", которую легко смывают затем обычной водой, а руку вытирают насухо полотенцем.
Примечание: Реакцию образования раствора роданида железа (III) можно использовать для получения хорошей имитации крови.
• Холодное пламя
Ингредиенты:
— сухая борная кислота, чайная ложка
— этиловый спирт, чайная ложка
— концентрированная серная или соляная кислота, одна капля
Все это помещается в блюдце, перемешивается и слегка подогревается на теплой (чтобы можно было держать руку) водяной бане. Выделяющийся эфир борной кислоты можно поджечь (не поднося спичку близко к блюдцу, чтобы не зажечь спирт). Эфир борной кислоты горит очень объемным, слегка зеленоватым пламенем, которое не только не обжигает, но даже не греет ощутимо, в нем спокойно можно держать руку, однако после того, как эфир борной кислоты весь выгорит, может начать гореть спирт, а его пламя действительно обжигает.
• Выделение кофеина из чая
Эксперимент основан на способности кофеина, подобно иоду, подвергаться возгонке (сублимации — свойство вещества при нагревании переходить в газ минуя жидкое состояние). Для проведения опыта необходимы две столовые ложки листового чая. Чай перетирают в ступке до мелкого порошка, затем переносят в сухую фарфоровую выпаривательную чашку, которая сверху накрывается большой стеклянной воронкой, причем края воронки должны выдаваться за края чашки примерно на 1 см. После этого нагревают чашку над пламенем горелки. Кофеин сублимируется и вновь конденсируется на воронке в виде белых кристаллов.
• Получение фенолформальдегидной смолы
В пробирку помещают 10 капель жидкого фенола и 8 капель 40 % формальдегида. Смесь нагревают на водяной бане до растворения фенола. Через 3 минуты в пробирку добавляют 5 капель концентрированной соляной кислоты и помещают ее в стакан с холодной водой. После образования в сосуде двух четких фаз следует слить воду и вылить полимер из пробирки. В течение нескольких минут образовавшаяся новолачная смола затвердевает.
• Получение искусственного шелка
Около 20 г гидрокарбоната меди растворяют в 25 %-ном растворе аммиака путем его постепенного добавления к соли и при постоянном помешивании. В полученный медно-аммиачный раствор вносят медицинскую вату небольшими порциями и перемешивают до полного растворения клетчатки и получения вязкой массы. Растворение ваты идет медленно, поэтому опыт можно отложить на 1–3 дня. Для получения нитей искусственного волокна медно-аммиачный раствор клетчатки набирают в медицинский шприц и выдавливают через иглу, погруженную в осадительный раствор, представляющий собой 10–15 %-ный раствор серной или соляной кислоты.
• Получение метана
Реактивы: Ацетат натрия (безводный!), гидроксид натрия.
Оборудование: Круглодонная колба, пробирка, лабораторный штатив (2), газоотводная трубка и пробка.
Методика:
В сухую пробирку или круглодонную колбу вносят тщательно прокалённый ацетат натрия CH3COONa и гидроксид натрия NaOH в соотношении 1:3 (по объему). Затем в пробирку вставляют пробку с газоотводной трубкой и, как обычно, проверяют прибор на герметичность. После чего, начинают нагревать смесь, сначала умеренно, затем более сильно. Образующийся метан СН4 собирают в пробирку методом вытеснения воды или воздуха, а затем поджигают. Газ сгорает подобно водороду — спокойно или со свистом — это зависит от чистоты полученного метана СН4.
Реакция:
CH3COONa + NaOH = Na2CO3 + СН4СН4 + 2O2 = 2Н2O + СO2
• Получение этилена и его свойства
Реактивы: Этанол (96 %), серная кислота концентрированная, перманганат калия, бромная вода.
Оборудование: Колба Вюрца (пробирка), спиртовка, прибор для собирания газов, ванночки с растворами (стаканчики).
Методика:
В пробирку или, что лучше в колбу Вюрца наливают 5 мл этанола и 2 мл серной кислоты. Смесь нагревают до 180°, при этой температуре начинает выделяться этилен (при более низкой температуре образуется эфир). Сначала этилен собирают в пробирку методом вытеснения воды и поджигают (газ легко сгорает). Затем газоотводную трубку прибора последовательно опускают в стаканчики или ванночки с раствором перманганата калия и с бромной водой. Наблюдают исчезновение (или значительное ослабление окраски).
Реакция:
С2Н5ОН +(H2SO4)= С2Н4 + Н2O
• Получение ацетилена
Реактивы: Карбид кальция, перманганат калия, вода.
Оборудование: Коническая колба, пробка с трубкой
Методика:
В коническую колбу объемом 100 мл кладут кусочек карбида кальция, наливают воду и затыкают пробкой с короткой трубкой. Сначала газ пропускают в подкисленный раствор перманганата калия, затем резиновую часть трубки снимают и поджигают ацетилен. Газ горит коптящим пламенем.
Реакция:
СаС2 + 2Н2O = Са(ОН)2 + С2Н2
• Свойства бензола
Реактивы: Бензол, перманганат калия, бром, азотная кислота (65 %), серная кислота конц., железные опилки.
Оборудование: Пробирки, химические стаканчики, делительная воронка
Методика:
1. Запах бензола. Учащимся дают понюхать в пробирке бензол, и объясняют, что название "ароматические углеводороды" на прямую не связано с запахом бензола.
2. Отношение к воде и перманганату калия. В химический стакан наливают раствор перманганата калия (не слишком концентрированный), а затем бензол. Смесь расслаивается, причем граница раздела двух фаз становится зеркальной, но перманганат не обесцвечивается.
3. Горение бензола (под тягой!). В фарфоровую чашку наливают 1 мл бензола и поджигают горящей лучинкой. Бензол сгорает ярким коптящим пламенем. Примечание: категорически советую проводить опыт под тягой — нашей школе пришлось отмывать потолок от копоти!
4. Бромирование бензола. В колбу с длинной вертикальной трубкой ("обратный холодильник") наливают 4 мл бензол и 2 мл чистого брома. Реакция не протекает. Затем в смесь на кончике ножа добавляют железных опилок и закрывают пробкой с холодильником. Начинается довольно бурная реакция, по окончании которой на дно оседает тяжелый слой бромбензола.
5. Нитрование бензола. В колбу с обратным холодильником наливают 8 мл концентрированной серной кислоты и 5 мл азотной (65 %). Полученную нитрующую смесь охлаждаю под сильной струёй воды. Затем добавляют 5 мл бензола. Смесь встряхивают. Если реакция пойдет медленно. Всплывающий желтый слой и есть нитробензол. Его можно отделить на делительной воронке и использовать для дальнейших опытов (получение анилина и др.).
Внимание! Нитробензол ядовит! (ТЯГА!)
Реакции:
2С6Н6 + 15О2 = 12СО2 + 6Н2О
С6Н6 + Вr2 = С6Н5Вr + НВr
С6Н6 + HNO3 = C6H5NO2 + Н2O
• Определение углерода и водорода в парафине
Реактивы: Парафин, оксид меди (2), сульфат меди (безводный), известковая вода.
Оборудование: Пробирки (2), штатив (штатив-держатель), пробка с газоотводной трубкой, спиртовка.
Методика:
В пробирку помещают оксид меди и парафин в объемном отношении 1:5. На её стенку аккуратно кладут обезвоженный сульфат меди, после чего, закрывают прибор пробкой с газоотводной трубкой и проверяют на герметичность. Смесь начинают осторожно нагревать. Когда парафин расплавится, трубку прибора опускают в известковую воду.
Нагревание продолжают 5-10 минут, при этом: известковая вода мутнеет, сульфат меди синеет, на дне пробирки образуются зернышки металлической меди.
Реакция: CnH2n+2 + (3n + 1)CuO = nСO2 + H2n+1O
• Горение этанола
Реактивы: серная кислота конц., перманганат калия, спирт.
Оборудование: Спиртовка, стеклянные пластинки, стеклянные палочки
Методика:
Горение спирта в принципе, не нуждается в демонстрации, однако если этот опыт поставить эффектно, то можно произвести благоприятное впечатление на учащихся, а заодно повторить курс неорганической химии.
На стеклянную или фарфоровую пластинку наносят немного кристалликов перманганата калия и прикасаются к ним стеклянной палочкой, смоченной в серной кислоте.
При этом образуется сильный, и к тому же взрывоопасный (!) окислитель — оксид марганца (VII).
Далее, стеклянную палочку подносят к фитилю спиртовки (фитиль должен быть мокрым), при этом спирт загорается.
Реакции:
2КМnO4 + H2SO4 = Мn2O7 + Н2O + K2SO4
2С2Н5ОН + 2O2 = 4СO2 + 6Н2O + Q
• Качественная реакция на многоатомные спирты
Реактивы: Глицерин (при отсутствии можно заменить сахорозой), раствор сульфата меди, гидроксида натрия.
Оборудование: Демонстрационные цилиндры
Методика:
В демонстрационную пробирку или цилиндр наливают немного глицерина (обратить внимание учащихся на вязкость глицерина — причины: обилие водородных связей, "маслообразность" — влияние углеводородной цепи) и разбавляют водой. В другом цилиндре готовят осадок гидроксида меди, смешивая растворы гидроксида натрия и сульфата меди. Содержимое цилиндров сливают вместе и перемешивают. Наблюдают образование соединения с красивой, "васильковой" окраской.
При подготовке учащихся к практическим работам опыт показывают в другой последовательности. В пробирку наливают раствор глицерина, добавляют гидроксид натрия (должен быть избыток), а затем сульфат меди. В этом случае, также наблюдается "васильковая" окраска, однако образование гидроксида меди не происходит, проведение опыта сильно упрощается, что важно для проведения практических работ.
Реакция:
СН2СНСН2(ОН)3 + Сu(ОН)2 = СН2СНСН2(OН)O2Сu (уравнение дано в упрощённом виде)
• Химические и физические свойства фенола
Реактивы: Фенол, лакмус или метилоранж, гидроксид натрия, соляная кислота, бромная вода, азотная кислота, хлорид железа (III)
Оборудование: Химические стаканы, демонстрационные пробирки, пробиркодержатель, спиртовка Методика:
1. К воде, налитой в химический стакан, прибавляют с помощью шпателя фенол и перемешивают смесь. Констатируют образование эмульсии, которая вскоре расслаивается. Объясняют, что нижний слой — раствор воды в феноле, верхний — раствор фенола в воде.
2. К части эмульсии полученной в предыдущем опыте прибавляют какой-нибудь индикатор. Среда — кислая. Значит фенол — кислота. Чтобы это подтвердить, к эмульсии прибавляют концентрированный раствор гидроксида натрия. Раствор становится прозрачным. На доске пишут соответствующую реакцию. Теперь, к полученному раствору фенолята натрия приливают раствор соляной кислоты. Снова образуется эмульсия, пишут уравнение, делают вывод о том, что фенол — кислота слабая.
3. Эмульсию фенола смешивают в демонстрационной пробирке с бромной водой. Выпадает белый осадок трибромфенола. Пишут реакцию, рассматривают взаимное влияние фенил-радикала и ОН-группы друг на друга.
4. Нитрование фенола. Опыт также иллюстрирует о, п-замещение в феноле. В пробирку насыпают немного фенола и расплавляют его (при этом демонстрируется его легкоплавкость — т. пл. 40 °C). После плавления смесь выливают в химический стакан с раствором азотной кислоты (2:3). При этом образуются различные продукты, в частности — пикриновая кислота (2,4,6-тринитрофенол — пикриновая кислота).
5. Качественная реакция на фенолы. Все фенолы с хлоридом железа (III) дают фиолетовое окрашивание.
• Качественное определение спиртов и фенолов
Реактивы: Парафин, оксид меди (2), сульфат меди (безводный), известковая вода.
Оборудование: Пробирки, штатив (штатив-держатель), пробка с газоотводной трубкой, спиртовка
Методика:
Задание: В трех предложенных вам пробирках находятся следующие вещества:
а) фенол
б) этанол
в) пропантриол-1,2,3
Используя предложенные реактивы, определите содержимое каждой пробирки Реактивы: Растворы гидроксида натрия, сульфата меди (II), хлорида железа (III)
• Получение альдегида
Реактивы: спирт этиловый, медная проволока.
Оборудование: спиртовка, химический стакан
Методика:
Из медной проволоки делают небольшую спиральку, которую раскаляют в пламени спиртовки и опускают в спирт. Эту операцию повторяют несколько раз. Полученный раствор обладает всеми свойствами альдегидов.
Реакция: СН3СН2ОН + CuO = СН3СНО + Н2O
• Реакция полимеризации формальдегида
Реактивы: формальдегид
Оборудование: демонстрационные пробирки, пробка с газоотводной трубкой, спиртовка
Методика:
В демонстрационную пробирку наливают 10 мл 40 %-ного раствора формальдегида. Пробирку начинают нагревать в пламени спиртовки. Раствор начинает мутнеть (образуется параформ — полимер формальдегида).
В другую пробирку насыпают немного сухого параформа, закрывают пробирку пробкой с газоотводной трубкой и начинают нагревать. В этом случае происходит мономеризация (деполимеризация) и образуется газообразный формальдегид (порошок улетучивается).
Реакция: nСН2O = (СН2O)n
• Получение фенолформальдегидной смолы
Реактивы: Фенол, формалин, соляная кислота (1:2).
Оборудование: пробирки, спиртовка, фильтровальная бумага
Методика:
В пробирку помещают смесь 2,5 г фенола и 5 мл формалина. Ничего не происходит. Затем добавляют 7-10 капель соляной кислоты (катализатор). При этом начинается катализатор. Смесь охлаждают и дают ей отстояться. При этом в зависимости от условий образуется либо желтая смола, либо кусочек уже твердой белой смолы.
• Реакция серебряного зеркала
Реактивы: Нитрат серебра (раствор 2 %), аммиак (раствор 25 %, разбавить в 8 раз), формалин (или другой альдегид), бихромат калия, серная кислота концентрированная (или готовая хромовая смесь).
Оборудование: ершик, пробирки, химический стакан, спиртовка, пробиркодержатель
Методика:
Для проведения реакции берут пробирку или колбу, два раза моют ее ершиком, промывают хромовой смесью и ополаскивают дистиллированной водой. Эта стадия подготовки очень важна, т. к. от чистоты сосуда зависит исход опыты.
В сосуд наливают на 1/4 раствор нитрата серебра и по каплям начинают добавлять раствор аммиака до полного растворения образовавшегося в начале осадка. К полученному раствору добавляют раствор альдегида. Полученную смесь аккуратно нагревают до потемнения растворы. Затем раствор выливают и показывают учащимся серебряное зеркало. Если зеркало не получилось, то не стоит браковать опыт: черный осадок это тоже серебро, только в виде мелкого порошка.
ПРИМЕЧАНИЕ: Аммиачную смесь не рекомендуется готовить заранее, т. к. при стоянии раствора в нем могут образоваться взрывчатые вещества — соли гремучей кислоты.
Реакция:
НСНО + Ag2O = НСООН + 2Аg
• Реакция с гидроксидом меди
Реактивы: гидроксид натрия, сульфат меди, раствор альдегида.
Оборудование: пробирки, химический стакан, спиртовка, пробиркодержатель
Методика:
В демонстрационную пробирку наливают раствор сульфата меди и добавляют к нему по каплям раствор гидроксида меди. Констатируют образование синего осадка гидроксида меди. Затем с осадка сливают часть жидкости и приливают к полученному осадку раствор альдегида. Смесь нагревают в пламени спиртовки, при этом происходит постепенное изменение окраски по схеме: синее-черное-зеленое-красное-желтое.
Реакция:
CuSО4 + 2NaOH = Cu(OH)2 + Na2SО4
НСНО + CuO = Cu2О + HCOOH
 ТЕЛЕГРАМ
ТЕЛЕГРАМ Книжный Вестник
Книжный Вестник Поиск книг
Поиск книг Любовные романы
Любовные романы Саморазвитие
Саморазвитие Детективы
Детективы Фантастика
Фантастика Классика
Классика ВКОНТАКТЕ
ВКОНТАКТЕ