Часть шестая Метилирование и преобразование
Способны ли биохимические факторы, отвечающие за уровень энергии, нетерпения и осторожности, стать причиной фиброзно-кистозных изменений в вашей груди и даже рака молочной железы? Представьте себе цепочку биохимических реакций, которая может вызвать приступы паники, мигрени, головные боли, аллергический насморк, проблемы с кишечником, крапивницу, боли в желудке и жалобы на рефлюкс.
Эта часть посвящена метилированию – реакции, которая каждую секунду протекает примерно в сорока триллионах наших клеток. После того как вы о нем узнаете, ваша жизнь не будет прежней. Его изучение помогло мне изменить свой подход к лечению и куда более эффективно бороться с болезнями, которые обычно считаются безнадежно хроническими.
Метильная группа – CH3, о которой я слышал на занятиях по биохимии в медицинском университете, невероятно важна с точки зрения реакций, в которые она вступает, и последствий ее дефицита в организме. Изучив все это, я понял, что нам с коллегами есть к чему стремиться. Я хочу поделиться тем, что узнал около восьми лет назад об этой цепочке реакций, благодаря чему смог преодолеть приступы бессонницы, продолжавшиеся месяцами, проблемы с вниманием и даже улучшить свой английский.
Весной 2013 г., как раз когда я учился справляться со всеми этими проблемами, общаясь со своим другом-врачом, я узнал, что несколько лет назад, в сорок, у него был сердечный приступ, что у него рецидивирующий тендинит[35] и приступы депрессии, резистентность к инсулину, которую он годами пытается преодолеть, и отсутствие желания вставать по утрам. На первый взгляд все эти симптомы не связаны друг с другом, но, зная о метилировании, я понял, что оно сыграет роль в преодолении проблем каждого из них. «Давай-ка проверим уровень гомоцистеина, а потом ген MTHFR», – сказал я. Он согласился, растерянно покачав головой. Как я и предполагал, показатель гомоцистеина, измеренный несколько раз, превышал 30, а ген MTHFR оказался с мутацией C677T, гомозиготным (оба гена, унаследованные от матери и отца, не работали в нормальном режиме).
В тот год в Турции достать необходимый ему витаминно-минеральный комплекс мне не удалось. По его словам, ему неплохо помогла подготовленная мной программа питания, которая включала комбинацию метилкобаламина, метилфолата, R5P, P5P и триметилглицина (этот препарат пришлось заказывать из-за границы), а также добавки магния и цинка в наиболее подходящей для организма форме. Одновременно с этим о положительных изменениях сообщил другой мой взрослый пациент. Вместо метилфенидата, в приеме которого он по собственному решению сделал перерыв, я предложил ему комбинацию омега-3, фосфатидилхолина, метилкобаламина и метилфолата, а также подобрал программу питания. Положительный результат еще больше усилил мой энтузиазм.
“Я чувствовал себя путешественником, который нашел собственный свет, отблески которого теперь помогали всем вокруг. Желание помогать и дальше было моей самой большой мотивацией”.
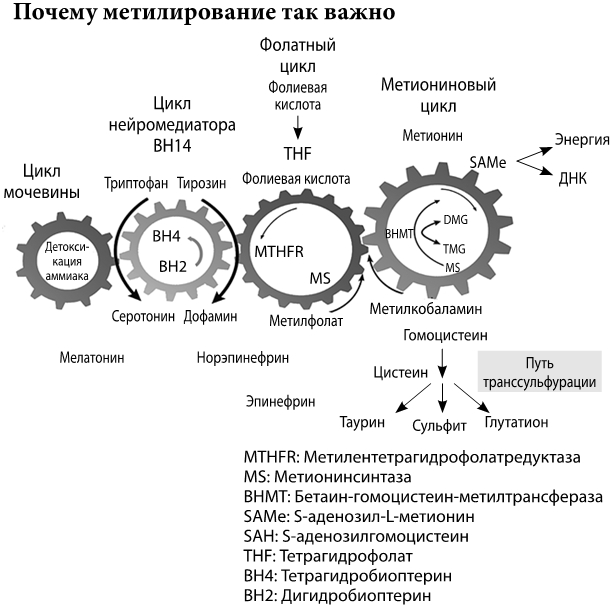
Рис. 12. Метилирование и связанные с ним циклы
Если бы я повесил перед вами гигантскую диаграмму со всеми важнейшими известными биохимическими циклами и попросил найти хоть один, который не затрагивал бы эту схему, это было бы очень трудно. Почему? Метилирование – это больше, чем перенос одноуглеродной метильной группы. С этим процессом очень тесно связан цикл фолиевой кислоты, с ним соседствует биоптерин, а с ним, в свою очередь, – жизненно важная биохимическая цепная реакция, путь транссульфурации. Каждый из этих циклов и путей, тесно взаимодействующих друг с другом, несет информацию и значение, которые можно изложить отдельной книгой.
Метилирование в каком-то смысле – это биохимический эпигенетический процесс. Эпигенетика использует супрагенетический подход. Проще говоря, эта концепция подчеркивает значение запускающей или останавливающей роли факторов окружающей среды в отношении генов. Это сильно отличается от подхода «одной переменной», который неосознанно обесценивает всю концепцию эпигенетики экспериментами на мышах, для которых он буквально прицельно выбирает внешние факторы.
“Влияние генов на нашу жизнь никак нельзя отрицать, но если удастся доказать, что даже небольшая метильная добавка или всасывание токсинов из кишечника, развитие резистентности к инсулину и лептину, воспаление, неполная детоксикация, гормональный дисбаланс могут серьезно повлиять на их рабочий потенциал, в медицине произойдет настоящая революция”.
Нам известна роль генетических предрасположенностей в развитии заболеваний, но благодаря опыту наблюдения за сотнями пациентов моей клиники нам, вероятно, удастся понять, как устранять коренные факторы таких заболеваний, как депрессия, диабет II-го типа и поликистоз яичников, выходя за рамки фаталистического генетического подхода.
Что такое метилирование?
Метилирование – это процесс передачи информации. Он имеет жизненно важное значение в целом ряде процессов: производстве и восстановлении РНК/ ДНК, в предотвращении рака (подавая сигнал «стоп» некоторым генам), в производстве миелиновой оболочки, которая чрезвычайно важна для быстрой нервной проводимости, в формировании фосфатидилхолина для структуры клеточных мембран, в выводе из организма норадреналина для управления тревогой, выработке коэнзима Q10 и карнитина для здоровья митохондрий – центра клеточной энергетической системы, преобразовании серотонина в мелатонин, устранении избытка гистаминов и выработке Т-лимфоцитов.
Основной источник метила в организме – SAMe, S-аденозилметионин. «Фабрика» по его производству – цикл трансформации метионина и гомоцистеина, который происходит в каждой клетке. Одна из основных целей медицины – обеспечить, чтобы этот цикл происходил стабильно и предоставлял достаточное количество SAMe. После того как SAMe переносит метильную группу, он превращается в S-аденозилгомоцистеин (SAH). SAH и SAMe – это конкурирующие молекулы. Очень важным параметром является соотношение SAMe/SAH, которое в норме должно быть в пользу SAMe. В противном случае SAH заблокирует все реакции, в которых должен участвовать SAMe.
“Уровень SAH, – возможно, один из лучших индикаторов риска повреждения сосудов, превосходящий даже гомоцистеин. Решающее значение имеет трансформация SAH в гомоцистеин, а затем в метионин, а метионина – в SAMe. Очень важно устранять блоки, возможные в этом цикле, и поддерживать альтернативные биохимические пути. Большая часть SAMe используется для образования креатина и фосфатидилхолина, которые включаются в структуру клеточной мембраны для производства энергии”.
При нарушении синтеза креатина затрудняется производство энергии. Если фосфатидилхолин не вырабатывается, проницаемость клеточных мембран и связи гормонов с клеточными рецепторами нарушаются. Вспомним, как нарушение клеточной связи соотносится с инсулинорезистентностью. Проблемы с выработкой фосфатидилхолина, если только его не вводить извне, могут привести ко многим неприятным клиническим состояниям, от резистентности к инсулину до ожирения печени и нарушения текучести желчи.
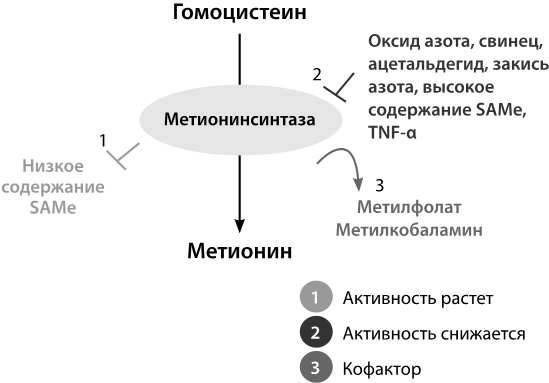
Рис. 13. Трансформация гомоцистеин-метионин
Некоторые известные нам функции метилирования.
• Производство креатина, необходимого для сокращения мышц.
• Синтез ДНК и РНК.
• Генная регуляция, запуск или подавление генов (эпигенетика).
• Гормональная регуляция и детоксикация (особенно эстрогена).
• Производство энергии (коэнзим Q10, карнитин, АТФ).
• Создание структуры клеточной мембраны (фосфатидилхолин).
• Жировой обмен.
• Производство миелина (оболочка нервных клеток).
• Производство иммунных клеток (Т-лимфоциты и NK-клетки).
• Производство и баланс нейромедиаторов.
• Функция сосудистого эндотелия и образование оксида азота.

Рис. 14. Цикл метилирования
Для здорового функционирования цикла требуется достаточное количество аминокислоты метионина и магния. После образования гомоцистеина АТФ необходимы метилкобаламин, метилфолат, цинк, а также здоровый функционирующий ген синтеза метионина. Для этой реакции очень важно, нет ли излишков перекиси водорода (H2O2), свинцово-ртутной токсичности, воспаления, резистентности к инсулину, проникания токсинов из кишечника в среду организма. Разберем на примере.
Неспособность человека с низкой кислотностью желудка правильно переваривать пищу может вызвать проблемы с образованием и всасыванием витаминов, минералов и аминокислот, необходимых для метилирования, также на метилировании серьезно отрицательно скажутся хронические проблемы с кишечником и воспаления, которые в долгосрочной перспективе ведут к проблемам с пищеварением. Метилирование связано не только с уровнем витаминов и минералов.
“Затронутые в каждом из разделов этой книги темы и процессы тесно связаны друг с другом. При воспалении, резистентности к инсулину и проблемах с детоксикацией сколько бы витаминов и минералов вы ни потребляли, проблему это не решит. Необходим комплексный подход, включающий регуляцию питания, внимательное обследование и лечение кишечника, поддержание обмена веществ, детоксикацию, метилирование и работу с психикой, если человек готов к ней”.
Около семи лет назад, когда я только начинал работать с метилированием, я рекомендовал большинству своих пациентов метилкобаламин, активную форму витамина B12. Метилкобаламин в то время был недоступен в Турции, и мои пациенты с кишечными проблемами выписывали из-за границы ампулы для подкожных инъекций, благодаря которым препарат попадал непосредственно в кровоток. И хотя это лечение, которое воодушевило меня как возможность быстро решить проблему, поначалу обеспечило очень хорошие и быстрые результаты для большинства пациентов, у небольшой группы препарат вызывал такие побочные эффекты, как сильное беспокойство, постназальное затекание, боль в суставах и мышечные судороги. Итак, необходимо признать, что метилкобаламин не для каждого пациента стал лучшим препаратом для коррекции дефицита витамина B12. Особенно если есть интенсивное воспаление, существует вероятность, что метильные группы направятся на путь транссульфурации (путь № 3), который становится выходными воротами для производства глутатиона, и увеличения количества некоторых побочных веществ (сульфита, аммиака), появление которых нанесет серьезный ущерб клетке, функции которой уже и так нарушены.
“Человек, плохо знающий свое тело, физиологию и процессы воспаления, может навредить себе, если по совету врача примет метилкобаламин”.
Могу с легкостью сказать, что невозможно достичь полноценного благополучия, не затрагивая питание, кишечник, систему обмена веществ и психическое здоровье организма. Цикл метилирования, общий для всех клеток, происходит по пути номер один, показанному на рисунке 13. Для работы этого пути необходимы активная форма B12, метилкобаламин и активная форма фолиевой кислоты, метилфолат. В присутствии этих двух активных витаминов гомоцистеин преобразуется в метионин. При блокировке пути № 1, то есть при недостатке этих активных форм или при интенсивном воспалении и окислительных повреждениях, метилирование осуществляется только по пути номер два. Это путь бетаин-гомоцистеин-метилтрансферазы. Для его функционирования (а также для образования метила) требуются молекулы триметилглицина и цинк. Если же нагрузка на этот путь очень велика и триметилглицина в организме недостаточно, для его работы начинает использоваться холин. Длительное функционирование метилирования через путь № 2 может вызвать серьезные проблемы, особенно в печени и желчном пузыре.
Зачем нам нужен витамин B12
Когда речь заходит о В12, сразу приходят на ум классические клинические состояния, такие как забывчивость, проблемы с равновесием и онемение рук и ног. Однако при таком дефиците возникает еще целый ряд симптомов: от снижения текучести желчи до резистентности к инсулину.
“В12 – не просто витамин, это еще и основа цикла метилирования, его дефицит приводит к сбоям в тысячах реакций. Оценивая его лишь в рамках числового показателя, мы теряем из виду его важные функции”.
Показатель содержания B12 в крови, взятой утром натощак, – это на самом деле общее значение кобаламина. Говоря о B12 как о чем-то одном, мы имеем в виду цианокобаламин, гидроксикобаламин, аденозилкобаламин и метилкобаламин. Измеренный показатель – сумма этих форм. Я часто сталкиваюсь с высоким уровнем В12 при высоком же показателе гомоцистеина. Такая ситуация свидетельствует о том, что бо́льшая часть B12 в крови на самом деле неработоспособна. Организм человека распознает и использует гидрокси-, аденозил– и метилформы В12 на протяжении десятков тысяч лет, а вот с цианокобаламином незнаком. Почти все витамины, которые сейчас продаются на аптечных полках нашей страны под названием В12, – это цианокобаламин. Эта форма, созданная с использованием цианида, – синтетическая, имеет длительный срок хранения и стабильна. Но когда недостаток В12 восполняют цианокобаламином, организм не может использовать его напрямую. Сначала цианидный фрагмент необходимо удалить с помощью глутатиона и превратить в метилкобаламин с метильной группой из SAMe или в аденозилкобаламин через АТФ. Я не останавливался на токсичности цианида, но не отдавал предпочтения этому варианту лечения в течение многих лет из-за его чужеродности для организма, цианидной нагрузки, которую он создает, и сложностей с выводом цианидной группы.
Другая форма B12 – гидроксикобаламин. Этот вариант B12 был моим основным выбором в период, когда активные формы в Турции не были доступны. Гидроксикобаламин неактивен, но он имеет ряд преимуществ перед цианокобаламином с точки зрения преобразования в активную форму. Кроме того, это естественная форма, и срок ее потребления также длительный. Также он выводится из организма гораздо быстрее, чем цианокобаламин. Для курильщиков с нитрозативным стрессом, вызванным радикалами оксида азота, и высокой цианидной токсичностью гидроксикобаламин – отличный выбор. Приятно радует и то, что в нашей стране он теперь доступен в безинъекционной пероральной форме.
“Могу с уверенностью сказать, что цианокобаламин – наиболее тяжелая для функционирования форма, особенно для человека с нарушениями цикла метилирования. Активные формы B12, действующие в прямых биохимических путях, – метилкобаламин и аденозилкобаламин. Форма B12, которая запускает цикл метилирования, – это метилкобаламин”.
Естественные формы В12 – это гидрокси-, аденозил– и метилкобаламин. Аденозилкобаламин – активная форма, расположенная в митохондриях. Он принимает участие в производстве энергии и синтезе жирных кислот, окружающих нервные структуры и образующих миелиновую оболочку. При рассеянном склерозе (РС) наши собственные иммунные клетки (особенно Т-лимфоциты) повреждают миелиновую оболочку нервных клеток. Нормальное функционирование метилирования – одна из немногих возможностей восстановить миелиновую оболочку, регулировать функции Т-лимфоцитов и сбалансировать иммунный ответ. С функциональной точки зрения анализ уровня B12 в крови не дает нам информации об объеме активных форм B12 и их успешном выполнении своих функций. Что ж, давайте копнем немного глубже: быть может, есть анализы, которые помогут нам получить представление о функциональной адекватности активных форм B12?
Метилкобаламин поддерживает образование метионина из гомоцистеина, обеспечивая здоровое функционирование фермента, называемого метионинсинтазой. Один из наиболее важных показателей, указывающих на дефицит метилкобаламина, – высокий уровень гомоцистеина. За сутки до измерения уровня гомоцистеина нужно перестать употреблять в больших количествах продукты с высоким содержанием белка (например, мясо и яйца). Для достоверного измерения важно, чтобы образец крови, взятый утром после двенадцатичасового голодания, был обработан в течение одного часа. Достаточный уровень метилкобаламина и метилфолата гарантирует, что гомоцистеин-метиониновый цикл протекает по пути номер один, показанному на рисунке 14. Преимущественно цикл метилирования в клетка идет именно этим путем. Аденозилкобаламин, другая активная форма B12, отвечает за активацию метилмалонил-КоА в митохондриях, центрах производства энергии в клетках. Этот фермент поддерживает образование АТФ, обеспечивая образование сукцинил-КоА из метилмалонового-КоА. Можно сказать, что аденозилкобаламин – это витамин В12 для митохондрий.
При дефиците аденозилкобаламина наблюдается повышение содержания метилмалоновой кислоты в моче. Он может проявляться такими симптомами, как мышечная слабость и хроническая усталость из-за дефекта выработки АТФ. Итак, чтобы понять концепцию дефицита B12, нужно выйти за рамки сугубо числовых данных. Изучив детали путей метилирования, мы понимаем, что витамины, минералы и добавки следует оценивать в комплексе и никакой панацеи не существует. Когда я читаю исследования, в которых оценивали при приеме В12 только его уровень, мне хочется задать их авторам тысячи вопросов: какую форму В12 принимали испытуемые, каковы были уровни гомоцистеина, было ли воспаление и можно ли его контролировать, шел ли цикл метилирования, каково было состояние митохондрий, достаточный ли был уровень метилфолата и магния, вырабатывался ли глутатион, каков, наконец, был режим питания? Так работает целостный подход.
“Основные правила целостного подхода заключаются в том, чтобы начать постигать функционирование организма на клеточном уровне, питание клетки, механизмы очистки от отходов, возникающих в клетке, и процессы коммуникации между клетками”.
Гомоцистеин – причина или следствие
S-аденозилгомоцистеин (SAH) образуется из SAMe, который использует свою метильную группу, а гомо-цистеин, серосодержащая аминокислота, образуется из SAH. На этапе образования цистеина существует несколько вариантов. Либо по классическому пути (путь номер один, показанный на рисунке 14) активная форма B12 преобразовывается в метионин под действием метилкобаламина и активной формы фолиевой кислоты через здоровую работающую метионинсинтазу с метилфолатом. Либо более коротким вторым путем, показанным на рисунке 14, – с участием бетаин-гомоцистеина с цинком и триметилглицином, когда метионин образуется посредством метилтрансферазы. Либо, как при третьем пути, поддерживается образование глутатиона, переходящего на путь транссульфурации. Если эти три пути находятся в равновесии, уровень гомоцистеина не увеличивается и обычно остается в пределах 6–8 мкмоль/л. Высокий уровень гомоцистеина почти всегда указывает на проблемы с циклом метилирования. В течение последних семи или восьми лет гомоцистеин – один из незаменимых параметров, которые я проверяю в результатах обследований своих пациентов. При высоком уровне гомоцистеина он может вызывать воспаление, создавая модифицированные виды белка, такие как тиолактон и N-гомоцистеин.
Гомоцистеин нейротоксичен, то есть повреждает нервные клетки. Также есть исследования, где его дисфункция связана с инсультом, резистентностью к инсулину и диабетической ретинопатией[36]. Воздействие на уровни асимметричного диметиларгинина, увеличение MMP9 и CRP могут нарушить внутренние связи системы, привести к усилению воспаления, сердечно-сосудистым заболеваниям и нарушить синтез коллагена, связанный с активацией фермента лизилоксидазы.
“Высокий уровень гомоцистеина – это главный показатель того, что жизненно важные биохимические процессы в организме нарушены. Помимо осознания факта, что проблемы, вызванные гомоцистеином, очень важны, главной задачей является осознание условий, вызывающих его повышение. Уверяю вас, если бы существовал препарат, который напрямую снижал бы уровень гомоцистеина независимо от того, как он повышался, сегодня мы все были бы гораздо лучше знакомы с понятием гомоцистеина. Очень рекомендую познакомиться с ним поближе. Как врач, регулярно наблюдающий уровень гомоцистеина у тысяч пациентов, могу сказать, что его вклад в работу организма огромен, если учитывать целостную структуру”.
У пациентки, с которой я проводил повторную беседу, потому что были проблемы в результатах других обследований, при первой беседе уровень гомоцистеина составлял 47 мкмоль/л. Дефицит витаминов и минералов и резистентность к инсулину, сопровождающие состояния, которые, вероятно, отрицательно влияют на активность генов (мутация одного гена, накопление тяжелых металлов, хроническое воспаление, окислительное повреждение), негативно сказываются на функционировании метилирования. Самой важной ее жалобой было затуманивание сознания. Она заявила, что ее восприятие на низком уровне, будто затуманено, а скорость мышления замедлилась. Из-за этого она не хотела выходить на улицу и встречаться с друзьями.
Многие больницы и частные врачи, к которым она обращалась с этими жалобами, согласились, что ситуация была психологической, «все анализы в норме» и что никакой «физиологической проблемы» не было. С моей точки зрения, у пациентки были серьезные проблемы с обменом веществ, значительное ожирение печени и уровень витаминов и минералов, который я мог бы описать как сносный. Это одна из ситуаций, с которой я часто сталкиваюсь в клинике и которая меня очень огорчает.
“Пациентка была в отчаянии, но при этом убеждена, что на физиологическом и биохимическом уровне все в порядке, хотя жаловалась на утреннюю усталость, подавленность, упадок сил и затуманенность сознания, которые крайне снижали качество ее жизни”.
Основные проблемы пациентки, нуждавшиеся в решении, были окислительное повреждение, воспаление, проблемы с питанием и кишечником, серьезный дефицит микроэлементов и проблемы цикла метилирования. Примерно за два с половиной месяца она пережила огромную трансформацию при моем участии, восполнив недостающие витамины и минералы, регулярно употребляя пищевые добавки, которые помогли решить проблемы с межклеточными связями и поддержать антиоксидантные функции, такие как пути образования глутатиона. В результате наших попыток понять и удовлетворить потребности ее тела у пациентки заметно возросла энергия, по ее словам, «увеличилась скорость мысли, разум стал намного яснее», она потеряла восемь килограммов, а уровень гомоцистеина снизился до 14 мкмоль/л. Можно сказать, что оптимальный уровень гомоцистеина находится в пределах 6–8 мкмоль/л. Но одно только это значение не дает нам достаточной информации о метилировании в организме. С другой стороны, если гомоцистеин высокий, это почти всегда указывает на наличие проблем.
Тогда с чем может быть связан низкий уровень гомоцистеина? Причиной может быть недостаточное потребление белка или же попытки клеток увеличить образование глутатиона при защитной реакции на хронически повышенный токсический фон или окислительное повреждение. Это один из механизмов самозащиты клетки. Для его реализации организм направляет гомоцистеин на путь номер три, а именно на путь транссульфурации, вместо пути номер один. Клетка делает это в ситуациях, когда есть угроза для нее самой, и в этом случае, даже если уровень гомоцистеина невысок, метилирование все равно может быть нарушено.
Метилирование и фолиевая кислота
Фолиевая кислота, как и B12, – это синтетический витамин, значение которого выходит за рамки его названия. Его естественная форма, присутствующая в организме, – фолат.
Как показано на рисунке 15, это молекулы, которые мы называем фолиевой кислотой, но на самом деле они сильно отличаются друг от друга с точки зрения функций. Слово «фолат» происходит от слова folium, что означает «лист». Зеленые листовые овощи – богатый источник фолиевой кислоты. Прежде всего, зеленые листовые овощи являются источником фолата. А фолиевая кислота – ее синтетическая форма. В норме после серии реакций фолиевая кислота превращается в конечный продукт 5-метилтетрагидрофолат (5-mthf, или метилфолат) и становится пригодной для использования в реакции метилирования. Следовательно, все реакции от фолиевой кислоты до синтеза метилфолата очень важны для эффективной работы цикла метилирования. В реакционной цепочке, ведущей от фолиевой кислоты к метилфолату, существуют две критические формы фолиевой кислоты. Первая – 10-формилтетра-гидрофолат, а вторая – 5,10-метилентетрагидрофолат. Эти молекулы играют активную роль в процессах образования ДНК/РНК. С этим свойством связано назначение фолиевой кислоты беременным женщинам с целью предотвращения у будущего ребенка возможных проблем, таких как дефект нервной трубки. Синтетические фолиевые кислоты, вводимые извне, нефункциональны, но если их преобразование достигается за счет ферментативных реакций, фолиевые кислоты переходят в активную форму и участвуют в необходимых процессах.

Рис. 15. Фолиевая кислота и метилирование
Прежде всего, для превращения фолиевой кислоты в фолат необходим фермент дигидрофолатредуктаза (DHFR). Если DHFR не работает должным образом из-за наследственности или вы подвергаетесь сильному воздействию тяжелых металлов, или принимаете такие лекарства, как метотрексат или сульфаниламиды, фолиевая кислота, которую вы принимаете извне, блокируется на первом этапе.
Последняя и основная реакция, в которой фолиевая кислота преобразуется в форму, используемую для метилирования (метилфолат), происходит с помощью гена-фермента метилентетрагидрофолата (MTHFR). MTHFR – это ген, важность которого я неоднократно наблюдал в ходе своего клинического опыта. Наиболее важной функцией этого гена, как следует из названия, является активация фолата посредством переноса метила. В гене MTHFR обнаружено около двадцати четырех мутаций. Среди этих мутаций особенно проблемная – C677T, которая создает высокий риск нарушений в цикле метилирования и образовании метилфолата. Если этот ген дефектно унаследован только от одного из наших родителей, он вызывает расстройство, называемое гетерозиготным, а если он унаследован с проблемами от обоих родителей, его называют гомозиготным. В исследованиях показывают нарушения функции примерно на 40 % в присутствии гетерозиготы MTHFR C677T и на 70 % – в присутствии гомозиготы MTHFR C677T. Существует множество генно-ферментных систем, связанных с метилированием. Я говорю именно об этом гене из-за того, что полиморфизм, влияющий на его функции, особенно распространен в Турции.
Больше всего в Турции этот ген исследуют клиники гинекологии и внутренних болезней. Это один из первых генов, который приходит на ум при выявлении выкидышей или тромбообразовании в венах, которое мы называем венозным тромбозом. Обычно в таких случаях мы ничего не можем сделать, кроме как рекомендовать пациентам разжижающие кровь препараты и фолиевую кислоту в синтетической форме. Но если организм уже не может эффективно превращать фолиевую кислоту в метилфолат, насколько функциональным может быть применение высоких доз фолиевой кислоты извне? Не ухудшат ли препараты ситуацию, нарушая перемещение метилфолата в клетку или его функциональность на уровне рецепторов?
“Итак, фолиевая кислота и В12 – жизненно важные молекулы, однако их значение для системы оправдывается, лишь когда они переходят в активную форму и становятся функциональны. Процессы их активации, функционирования и влияющие на эти процессы факторы необходимо тщательно изучать”.
В поисках исследований по MTHFR вы встретите публикации, в которых говорится о многих заболеваниях и взаимоотношениях генов. Если подойти к вопросу с несколько иной точки зрения, то возможным результатом дефекта гена MTHFR C677T является неспособность образовывать метилфолат в конечной точке пути фолиевой кислоты. Давайте еще раз вспомним, что сердцем цикла метилирования является реакция, в которой гомоцистеин превращается в метионин в присутствии метилфолата (5-mthf), метилкобаламина и здоровой функционирующей метионинсинтазы (MS).
“Ген MTHFR C677T, обладающий потенциалом существенно влиять на реакции метилирования, играет важную роль во многих корневых реакциях, включая образование карнитина, переносящего жиры в митохондрии, образование фосфатидилхолина, обладающего способностью влиять на все системы связи, присоединяясь к структуре клеточной мембраны, детоксикацию эстрогена, который теряет свою канцерогенность (повреждение ДНК) при метилировании, и синтез мелатонина – одного из важнейших внутриклеточных антиоксидантов”.
Я вижу наследственные проблемы с геном MTHFR почти у всех пациентов, и, если закрадываются подозрения, прошу их пройти обследование. Однако в рамках этого раздела я должен рассказать еще кое-что. В 2013 г., когда меня невероятно волновали проблемы метилирования, было трудно не рекомендовать каждому первому пациенту тестирование MTHFR. Частота моих запросов на этот тест снизилась за последние три или четыре года. Вы спросите, почему? «Топливом» фермента MTHFR является витамин B2, и некоторые врачи-исследователи совершенно уверены, что дефицит B2 (рибофлавина) гораздо важнее, чем эти генные мутации. Я не столь настойчив в этом вопросе, но одна из первых добавок, которые я даю своим пациентам, когда у них высокий уровень гомоцистеина, – это R5P, активная форма витамина B2. Если еще немного углубиться в тему, мы узнаем следующее.
“Чтобы все активные или подавленные генно-ферментные системы в организме, включая MTHFR, работали на высшем уровне своего унаследованного «переданного» потенциала, необходима программа правильного питания, здоровая пищеварительная система, микробный баланс в кишечнике. Нам необходимо метаболическое и митохондриальное здоровье, контролируемое воспаление и сбалансированный цикл метилирования”.
Думаю, вы получили представление о цикле метилирования, биохимических путях выработки метила в организме. Поговорим теперь о том, где мы используем эти метильные группы.
Синтез фосфатидилхолина
Если вы впервые слышите о фосфатидилхолине, можете быть уверены, что эта информация вам пригодится. Почему? Что ж, остановимся подробнее на упомянутых ранее моментах.
В организме триллионы клеток, и у каждой клетки есть мембрана, которая обеспечивает связь и обмен с внешним миром, а также защищает клетку от токсичных веществ. Название этой мембраны – клеточная мембрана.
Представьте, что вы заперлись дома, наглухо забили двери и окна и полностью отключили связь с внешним миром. Или, наоборот, что дверь и окно всегда открыты, в дом заходят посторонние и животные, которые портят дом, и нет механизма, который мог бы это предотвратить. В обоих случаях мы могли бы столкнуться с серьезными проблемами. То же и в клетке: если клеточная мембрана цела, ядро внутри клетки и ее содержимое, ДНК и митохондрии, являющиеся электростанциями, имеют шанс быть в безопасности. Отсутствие клеточной мембраны приводит к гибели клетки.
Фосфатидилхолин – фосфолипид, который является основным веществом, содержащимся в структуре клеточной мембраны.
• Если в мембранной структуре недостаточно фосфатидилхолина, клетка не может распознавать и получать необходимые ей микроэлементы. Сколько витаминов и минералов ни принимай, если клеточная мембрана не может выполнять свою работу и связи с рецепторами нарушены, клетка будет голодать, даже если вы сыты.
• Знаете ли вы, что примерно двести двадцать миллиардов наших клеток умирают и восстанавливаются каждый день? В каком-то смысле производство клеток также означает потребность в фосфатидилхолине. Эта потребность еще больше возрастает в период роста, грудного вскармливания и беременности.
• Фосфатидилхолин обеспечивает текучесть желчи и предотвращает состояние, называемое сладжем[37]. Желчная жидкость предотвращает размножение микробов, особенно в тонком кишечнике, где всасывание интенсивно. При СИБР желчь является важным защитным фактором.
• Фосфатидилхолин играет роль в переработке и удалении триглицеридов в печени. При его дефиците значительно возрастает склонность к ожирению печени.
• Фермент, необходимый для образования фосфатидилхолина и холина, – это фосфатидилэтаноламин-метилтрансфераза (PEMT). Метильная поддержка является критическим фактором для здорового функционирования этой генно-ферментной системы. При наличии нормального метилирования большая часть образующихся метильных групп (70 %) будет перенесена в эту реакцию.
• Холин отвечает за функции печени, нервной системы, движение мышц и выработку ацетилхолина (активно задействован, когда мы находимся в процессе обучения и концентрации).
• Одной из наиболее важных добавок, обеспечивающих достаточный уровень фосфатидилхолина в организме, является холин.
Очень важно получать достаточное количество холина с пищей. Печень, яйца, курица, рыба и красное мясо надежного происхождения – лучшие источники холина и наиболее важные добавки для поддержки метилирования. Вегетарианская и веганская диета остаются факторами риска дефицита холина. Спаржа, красная свекла, шпинат, брокколи, киноа и льняное семя – альтернативные добавки, богатые холином.
• PEMT работает более эффективно в присутствии эстрогена. Поэтому недостаточное потребление холина частично переносится молодыми женщинами, но не мужчинами. Им важно регулярное потребление холина. Также оно имеет решающее значение для женщин в постменопаузе, особенно для здоровья печени.
• Если PEMT не работает должным образом, возможны такие симптомы, как усталость, мышечные боли, ожирение печени, проблемы с желчным пузырем, мышечная слабость, высокий уровень триглицеридов (стоит сказать, что любой фактор, отрицательно влияющий на цикл метилирования, может привести к таким результатам).
Непереносимость гистамина и метилирование
Прежде чем разобраться в этом вопросе, давайте рассмотрим ситуацию, которая еще не попала в центр внимания и заставляет врачей из самых разных отраслей пожимать плечами. Вот пример: тревожность, колебания артериального давления, гастроэзофагеальный рефлюкс, цикл диарея-запор, которые были спровоцированы расставанием во время учебы в университете, – все эти симптомы сорокаоднолетней Элиф Ханым продолжались примерно двадцать два года. Два независимых психиатра диагностировали у нее «панику», основываясь на том, что, помимо прочих симптомов, она страдала от головных болей разной степени тяжести, хроническим насморком, трудностями с удержанием внимания и зудом. Также она жаловалась на крапивницу, которая иногда, – по ее мнению, из-за стресса, – требовала применения кортикостероидов, а в последние два с половиной года на эти симптомы наложилось значительное беспокойство перед менструациями, проблемы с потерей веса и болезненность молочных желез. Почти всегда симптомы появлялись одновременно. У нее были следующие диагнозы: паническое расстройство, мигрень, головная боль напряжения, синусит, синдром раздраженного кишечника, рефлюкс, крапивница. Она находится под регулярным наблюдением четырех врачей-специалистов и принимает назначенные лекарства.
В самом начале нашей встречи с госпожой Элиф мне пришло в голову, что, возможно, существует проблема, связанная с гистамином, поскольку история, которую она рассказала, соответствовала моей собственной истории. Я хочу, чтобы вы знали, что почти все эти жалобы, которые на протяжении многих лет пытались периодически и ограниченно купировать разными способами, могут быть связаны с непереносимостью гистамина. Когда ей пришлось обратиться в отделение неотложной помощи после употребления варившегося в течение суток костного бульона, рекомендованного в одной из социальных сетей в материалах о здоровом образе жизни, за которыми она следила, это дало серьезную информацию о клинической картине.
Наш организм существует в балансе. Даже самое важное для здоровья вещество может вызвать проблемы, если будет присутствовать в слишком большом количестве. Гистамин – практически идеальный пример. Он играет очень важную роль в секреции желудочной кислоты, которая является одним из ключевых моментов пищеварения, стимуляции иммунной системы и перистальтики кишечника при воздействии микробного агента. Короче говоря, гистамин необходим для здоровой иммунной системы, а также пищеварительных и выделительных процессов.
Представьте, что у вас внутри ведро, полное гистамина. Когда уровень этого вещества, которое мы и вырабатываем, и потребляем, и тратим, выходит из равновесия, то есть когда ведро начинает переполняться, иммунная система срабатывает неправильно. Увеличение гистамина в пищеварительной системе ведет к дисбалансу дефекации. Здесь вступает в игру важный фермент – диаминоксидаза (ДАО). В ответ на повышение уровня гистамина она попытается разрушить избыток. На ДАО отрицательно влияет препарат метформин, который часто назначают, особенно при резистентности к инсулину. Если у тех, кто принимает метформин, возникает вздутие и напряжение живота, стоит предположить, что количество гистамина у них увеличилось, потому что ДАО не может работать эффективно. Антациды, антибиотики и ингибиторы моноаминоксидазы также оказывают негативное влияние на ДАО.
“Кальций и медь в значительной степени способствуют эффективному функционированию ДАО. Говяжья печень, миндаль, чечевица и семена подсолнечника являются важными источниками меди, руккола, укроп, крапива – кальция”.
Что такое гистамин
Как мы получаем гистамин? В первую очередь, с аминокислотой гистидин, содержащейся в белках, которые мы едим. Важную роль играют также вещества, которые превращают гистидин, который мы поглощаем, в гистамин. Продукты с высоким содержанием гистамина также являются важным фактором, увеличивающим гистаминовую нагрузку. К продуктам, содержащим большое количество гистамина, относятся:
• соленья, содержащие живые бактерии;
• йогурт;
• кефир;
• сыр;
• сушеное мясо.
Нужно помнить также, что костный бульон, один из самых питательных и здоровых продуктов, может значительно повысить уровень гистамина. Также и употребление алкоголя у человека с непереносимостью гистамина не только увеличивает гистаминовую нагрузку, но и может привести к переизбытку гистамина за счет снижения активности фермента ДАО.
• Гистамин расщепляется внутри клетки ферментом гистамин-N-метилтрансферазой. Как следует из названия, этот фермент использует метильную группу. По мере увеличения количества гистамина потребность в метиле увеличивается.
• Из-за переизбытка гистамина могут наблюдаться такие симптомы, как постназальный затек, чихание, насморк, повышенная тревожность, дисбаланс артериального давления, приступы головной боли, нарушения перистальтики кишечника, кожный зуд и сыпь.
Речь идет больше о способности организма справляться с повышенной гистаминовой нагрузкой, чем о чувствительности к какой-либо конкретной пище. Следовательно, одна и та же пища может оказывать различное воздействие в разные дни и в разных условиях. Сравните человека с чувствительностью к глютену, который может испытывать проблемы после каждого его употребления, и человека с непереносимостью гистамина, который пьет домашний яблочный уксус. Второй не всегда испытывает одинаковую чувствительность к гистамину.
• Вспомним теперь и об антигистаминных препаратах. Поскольку в данном случае проблема – гистамин, подействуют ли они? Механизм действия этих препаратов осуществляется на уровне рецепторов. Например, при аллергическом процессе вы заблокировали H1-рецепторы. Это задерживает последствия воздействия гистамина на рецептор на время действия препарата, но не влияет на общий уровень гистамина. Другими словами, эти препараты блокируют гистаминергическую реакцию, но не уровень гистамина. А ведь именно его повышение – корень проблемы, и, если мы не разберемся с коренными факторами, которые наполняют «ведро» гистамина, придется искать врачей других специальностей и другие лекарства для решения проблем, которые могут возникнуть в системах, где препарат неэффективен. Это все равно что давать антацид (блокатор H2 или ИПП) при повышении кислотности желудка, которое происходит в ответ на переизбыток гистамина.
• При переполнении «ведра» с гистамином очень трудно лечить синдром повышенной проницаемости кишечника и размножение микробов в тонком кишечнике, то есть СИБР.
• Если необходимо использовать пробиотики, следует быть очень осторожным при выборе вариантов и знать, что особенной осторожности требуют пробиотики Lactobacillus casei и Lactobacillus bulgaricus, поскольку они вызывают повышение уровня гистамина. Бифидобактерии и Lactobacillus plantarum – добавки, которые могут помочь нам при непереносимости гистамина.
• При доминировании эстрогена секреция гистамина может увеличиваться. Если гистаминергические жалобы усиливаются у женщин в период овуляции (дни 10–14 при цикле 28 дней), то один из основных факторов, которые нужно рассмотреть, – это гормональный дисбаланс.
• Очень важно регулировать питание так, чтобы не повышать гистаминовую нагрузку, избегать чрезмерного потребления белка, употреблять свежие продукты. Свежее мясо и рыба, фрукты, кроме цитрусовых, куриные яйца от кур на свободном выгуле, гречка, киноа, кокосовое молоко, миндальное молоко, оливковое масло, помидоры и овощи, кроме баклажанов, входят в группу, которую мы в целом можем назвать безопасной. Яблочный уксус, произведенный традиционными методами в подходящих условиях, – один из продуктов, которые я рекомендую попробовать. Советую начинать с очень малых объемов и, если чувствительности не окажется, можно продолжать. Приготовление или проращивание обычно не снижают уровень гистамина в продуктах. Поэтому лучший способ – это ограничить их.
• Если необходимо поддержать процесс пищеварения, серьезный вклад внесут желудочная кислота, ферменты поджелудочной железы и желчные добавки. Неконтролируемый стресс вредит всем этапам пищеварения. Регулирование сна и физические упражнения способствуют процессу выздоровления во всех смыслах.
• Здоровое функционирование цикла метилирования – незаменимый фактор для удаления переизбытка гистамина. Так что теперь мы лучше знаем важные детали, необходимые для правильной работы цикла.
• Витамин С, P5P (активная форма витамина B6), медь и кальций – важные микроэлементы, которые играют роль в выведении гистамина.
Метилирование и детоксикация эстрогенов
Может ли нарушение цикла метилирования или выработки метила привести к серьезным проблемам, таким как рак молочной железы и рак эндометрия матки? Готовьтесь, мои дорогие читатели! Вы собираетесь изучить один из предметов, который перенесет вас за пределы времени.
Эстроген – женский гормон, выполняющий важные функции в организме. Уровень эстрогена, о котором мы более подробно говорили в разделе «Гормональный баланс», должен находиться в определенном балансе. Эстроген имеет большое значение, если рассматривать его с точки зрения целостного подхода. Он принимает участие во многих реакциях: от воспроизводства и здорового функционирования женских половых органов до здоровья сердца и сосудов головного мозга, баланса липидного профиля, защиты от остеопороза, а также способствует выработке коллагена и фосфатидилхолина. Итак, поговорим о том, как выводится эстроген из организма, какие стадии этого процесса известны и какова здесь функция метилирования?

Рис. 16. Метаболизм эстрогена
Наиболее физиологически активной формой эстрогена является эстрадиол. Очень важна детоксикация эстрона, который преобладает после менопаузы. В процессе детоксикации очень важно определить, какова нагрузка эстрона (Е1) и эстрадиола (Е2) на организм и достаточно ли функциональна у вас система для обработки, упаковки и выведения существующего объема через мочу и кал.
Ранее мы говорили о процессах детоксикации печени фазы 1, фазы 2 и фазы 3 – транспортной. Здесь мы снова сталкиваемся с этой системой. Реакции 1-й фазы эстрогена (особенно эстрона и эстрадиола) в печени в основном осуществляются ферментами цитохрома, начиная с CYP, который мы и называем цитохромом. Особенно важную роль играют метаболизм эстрогенов и цитохромные реакции, происходящие в молочной железе. Это своего рода предварительная обработка, проводимая до того, как из организма выводятся лекарства, яды и гормоны.
На рисунке 16 мы видим вверху ферменты CYP1A1 и CYP1B1. Эти ферменты преобразуют гормон эстроген через CYP1A1 в 2-гидроксиэстрон (2-OHE1), 2-ги-дроксиэстрадиол (2-OHE2). Он также производит 4-гидроксиэстрон (4-ОНЭ1) и 4-гидроксиэстрадиол (4-ОНЭ2) посредством CYP1B1. Одна из наиболее важных деталей, на которую следует обратить внимание, заключается в том, что эти новые биохимические молекулы теперь оказывают совершенно иное воздействие, чем эстроген. Следует подчеркнуть, что путь CYP1B1, который приводит к образованию 4-ОНЕ1 и Е2 при метаболизме эстрогенов, несет в себе серьезные риски для организма. После образования 4-OHE1 и E2, если у вас есть поддержка метил-CH3 (SAMe), которую вы получаете благодаря здоровому рабочему циклу метилирования, 4-OHE1 и 4-OHE2 могут быть метилированы и удалены из системы во время второй фазы детоксикации. Образующиеся метоксиэстрогены являются предвестниками безопасного для нас биохимического процесса. Некоторые расширенные тесты (голландские) позволяют даже измерить соотношение метилированных и неметилированных эстрогенов в моче. Не прибегая к каким-либо тестам, я могу сказать, что у десятков людей вокруг нас, у которых уровень гомоцистеина в крови составляет около 15–20 мкмоль/л и чьи клетки испытывают недостаток B12 и магния, нет возможности метилировать.
“Для передачи метильной поддержки нужен генетически здоровый фермент катехол-о-метилтрансфераза (КОМТ). «Топливом» КОМТ являются метильные группы, а магний – незаменимый минерал для ее работы”.
КОМТ, или фермент катехол-о-метилтрансфераза, детоксифицирует «опасные» метаболиты эстрогена, содержащие катехоловое кольцо, путем метилирования их в присутствии достаточного количества SAMe, а также играет важную роль в работе центральной нервной системы. Например, он участвует в поддержании баланса норадреналин-дофамин, который содержит катехиновое кольцо. Если баланс норадреналин-дофамин смещается в пользу норадреналина, мы чувствуем тревогу, нервозность и беспокойство. Другими словами, ферменту КОМТ принадлежит важнейшая функция в выведении норадреналина. И наоборот, при постоянной тревоге и беспокойстве вы тратите много КОМТ, метильных групп и магния. Что происходит при дефиците метила, когда КOMT не активируется?
Промежуточные эстрогены, которые появляются в наших клетках, подвергаются окислению при отсутствии или недостатке метила с образованием 4-ОНЭ1, производных хинона Е2 и семихинона. Все эти конечные продукты чрезвычайно канцерогенны. Они прочно связываются с ДНК и изменяют ее.
“Образовавшийся мутаген, то есть канцерогенная молекула, является источником большого риска не только для тканей молочной железы и эндометрия, но и для всего организма”.
Мы были бы неправы, если бы думали, что то, о чем мы говорим, касается только женщин, ведь есть серьезные доказательства того, что это состояние увеличивает риск рака простаты у мужчин. Хинонредуктаза, обозначенная на рисунке как NQO1, является наиболее важным антиоксидантным ферментом, который защищает нас от этих канцерогенных производных эстрогена. Существует два способа восстановления 4-OHE1 и 4-OHE2 в форме хинона и семихинона: они либо повторно гидроксилируются хинонредуктазой, либо удаляются глутатионом.
Уменьшение окислительного повреждения, то есть обеспечение митохондрий «чистым топливом», восстановление проницаемости стенок кишечника, прием антиоксидантных добавок, борьба с воспалением, регулирование питания, прием экстракта листьев оливы, содержащего мелатонин, N-ацетилцистеин, опеуропеин, танины и олеаноловую кислоту, послужат не только детоксикации эстрогена, но и комплексной поддержке ферментной системы. Индол-3-карбинол (I3C), обнаруженный в брокколи, цветной капусте и капусте, производит дииндолметан (DIM) при воздействии достаточного количества желудочной кислоты и подавляет канцерогенный путь CYP1B1. Эти две молекулы доступны в виде пищевых добавок. Важность глутатиона и его связь с метилированием будут объяснены в отдельном разделе.
Хотя эта теоретическая информация может показаться некоторым из нас немного запутанной, попытаюсь вкратце объяснить, как может эстроген, незаменимый гормон, превратиться в канцерогенную молекулу.
Представьте, что вы эстроген, у вас есть три варианта первого отпуска с супругом и ребенком. Отношения с родителями супруга у вас не очень хорошие, как и отношения супруга с вашими родителями. И вы, и ваш супруг хотите навестить каждый своих родителей, у которых не были уже три отпуска. Третий вариант – поездка в Гёбекли-Тепе, которую вы все откладывали, хотя уже давно собирались. Попадание в среду, где один из партнеров будет плохо себя чувствовать, – это путь CYP1B1, то есть 4-OHE1, E2. Трудный путь. Если вы миритесь с ситуацией, чтобы ваш партнер или кто-либо еще не пострадал или не расстроился, – это воспаление.
Если вы находитесь под давлением супруга, это метаболические проблемы, выражающиеся в лептинорезистентности. У пациентов это выражается частым чувством голода, они вынуждены питаться пять-шесть раз в день, а обхват талии у них выше 100 см. Допустим, вы начали этот путь как эстроген, неохотный, беспокойный, немного злой, «пытающийся выглядеть так, будто проблем нет», но, с другой стороны, готовый взорваться, с мечтой о Гёбекли-Тепе, застрявшей на одной стороне тела. У вас проблемы со свекровью, которая к вам холодна и отстранена, ни разу не смотрела вам в глаза с того момента, как вы вошли в ее дом, и каждое ее действие внушает вам ощущение никчемности, впервые возникшее еще на свадьбе. Выздоравливайте скорее, мой дорогой читатель! Теперь вы «окислились», превратились в хинонированный эстроген, и вы больше не «вы, какими вы себя знаете». С этого этапа вы потеряли контроль, это ваше самое токсичное и канцерогенное состояние.
Важны также факторы, существовавшие в домашней обстановке до того, как вы потеряли контроль. Если ваш свекр – человек, способный снимать напряжение, внушать чувство безопасности, а также обеспечить близость и сострадание, которые ваш отец внушал вам в детстве, это ваша «хинонредуктаза». Она может помочь почувствовать, что вы достойны любви и принадлежите этому месту, позволяя вам испытать противоположность негативным эмоциям, которые у вас уже есть и которые вызывает свекровь. В этой ситуации вы не создали проблем, но недовольны тем, в какой среде находитесь. Допустим, ваш партнер понимает чувства, которые вы испытываете все это время, не критикуя, не обесценивая и не осуждая вас, а понимая и принимая ваши эмоции, и решает посвятить остаток отпуска поездке в Гёбекли-Тепе. Вы счастливы, теперь вы – «метилированный неопасный» эстроген. Итак, путь, по которому мы идем, с кем мы находимся на этом пути, и наша история – важнейшие факторы, влияющие на наше самочувствие в настоящий момент. Конечно, это пример не без доли юмора. Это отражение моего ощущения, что клетки, нейрональные посредники, ферменты, гормоны и гены – такие же существа, как и мы, и что все они имеют свои собственные «привычки и проблемы».
Метилирование, глутатион и мелатонин
«Человек – существо, отравленное кислородом». Удивиться после прочтения этого предложения вполне нормально. Потому что вы знаете, что без кислорода нет жизни, и это абсолютно верно. Энергия, возникающая в результате сжигания потребляемой нами пищи, переваривания и всасывания из кишечника в насыщенной кислородом среде внутри митохондрий, дала нам возможность стать теми, кто мы есть. Если это чудо – результат длительной адаптации, продолжавшейся миллионы лет, можем ли мы адаптироваться и к той экосистеме, в которой живем сейчас? Все это лирика, вернемся к вопросу: отравляет ли нас кислород?
Свободные радикалы кислорода помогают клеткам производить большое количество энергии (АТФ).
Хотя в небольших количествах эти молекулы оказывают положительное воздействие, они чрезвычайно вредны для митохондрий, клеточных мембран и ДНК, когда достигают высоких уровней. Избыток кислорода может нарушить структуру клеток, что приведет к их гибели или неконтролируемой пролиферации. Когда нарушается баланс свободных радикалов кислорода и антиоксидантной системы, увеличивается восприимчивость к десяткам заболеваний. Главным внутриклеточным антиоксидантом клетки является глутатион. Всем, у кого есть жалобы, которые звучат так: «Я не хочу заболеть раком, в моей семье были болезнь Альцгеймера, Паркинсона и рассеянный склероз. Я боюсь. Я не хочу стареть. Я хочу решать судоку в девяносто лет. Я хочу вылечить печень и избавиться от депрессии. Большую часть своей жизни я провел с заболеваниями иммунной системы. Я очень часто болею. Почему не проходят синяки под глазами?» – необходимо знать о глутатионе. Каждый, кто читает эту книгу, должен понимать, что важна не болезнь как таковая, а основные факторы ее появления.
Глутатион – самый мощный антиоксидант клетки, состоящий из глицина, глутамина и цистеина. Он участвует и в процессах детоксикации. В синтезе глутатиона цистеин участвует в качестве ограничителя скорости реакций образования глутатиона. Мы знаем, что добавки N-ацетилцистеина повышают уровень глутатиона. Как видно на рисунке 12, одним из трех путей, по которым может перемещаться гомоцистеин, является путь транссульфурации. Мы можем синтезировать цистатион из гомоцистеина и цистеин из цистатиона.
Наиболее важными опорами этого пути являются витамин B6 (p5p), цинк, магний и глицин. Присоединится ли цистеин к структуре глутатиона или превратится в таурин и очистится, решается в клетке в зависимости от ситуации окислительного стресса.
“Предположим, у вас в организме достаточно цистеина и нет окислительной нагрузки. Вместо глутатиона цистеин создаст таурин, антиоксидант и нейрональный мессенджер, который защищает центральную нервную систему от стимулирующих воздействий, то есть поддерживает ее в покое, а также участвует в формировании структуры желчных кислот, способствует снижению уровня ЛПНП у пациентов с ожирением и диабетом и защищает сосудистые структуры (эндотелий)”.
Система работает совершенно по-разному при наличии или отсутствии угрозы. Путь транссульфурации особенно активен при окислительных повреждениях и воспалении и стимулирует выработку глутатиона. В этом случае цикл метилирования не запускается и использует путь № 3, пока уровень угрозы не изменится в лучшую сторону. Фактически это можно рассматривать как защитный механизм для краткосрочной перспективы. При наличии длительного клеточного стресса также возможно, что гомо-цистеин окажется на очень низком уровне. Помимо цистеина, в последнее время на первый план вышло негативное влияние дефицита аминокислоты глицина на образование глутатиона. Помимо участия в структуре глутатиона, глицин также играет роль в образовании коллагена, креатина, желчи и гемоглобина, который играет роль в транспорте кислорода. Говядина, курица и яйца являются хорошими источниками цистеина (если у вас нет проблем с пищеварением или всасыванием), а мясо, рыба, желатин, бобовые богаты глицином.
“В присутствии здоровой функционирующей глутатионпероксидазы глутатион может превращать H2O2 (перекись водорода) в воду. Он предотвращает как вредное воздействие перекиси водорода, так и возможное образование опасных гидроксильных (—ОН) групп. «Топливом» глутатионпероксидазы, то есть ее незаменимым ингредиентом, является селен”.
Это одна из причин, по которой я измеряю уровень селена в сыворотке крови у всех пациентов. Поскольку после этой реакции глутатион окисляется, его нельзя использовать повторно. Глутатион может вернуться в свое функциональное состояние в присутствии глутатионредуктазы и витамина B2. Методы вроде измерения соотношения восстановленных окисленных форм глутатиона для его функциональной оценки пока не кажутся очень практичными. Наиболее важным показателем роста потребности в глутатионе в анализе крови является повышение уровня фермента ГГТ (гамма-глутамилтрансфераза). Следует подчеркнуть, что проявить осторожность нужно, уже когда уровень этого фермента, который пытается активировать выработку глутатиона аминокислотами, превышает 25 ед/л, а не диапазоны, указанные в лабораторных рекомендациях.
Что нужно сделать, чтобы глутатион вырабатывался и функционировал? Мы знаем, что основные правила – это нормальный цикл метилирования, борьба с воспалением, поддержание метаболического баланса, устранение проблем с пищеварением и кишечником, а также управление стрессом. Попытка компенсировать дефицит прямым добавлением глутатиона весьма спорна, особенно из-за возможности превращения «восстановленных» форм глутатиона в окисленные формы в определеных условиях. Весьма вероятно, что в ближайшие годы липосомальные формы глутатиона выйдут на первый план с точки зрения эффективности на клеточном уровне. С точки зрения поддержки образования глутатиона N-ацетилцистеин и альфа-липоевая кислота являются теми добавками, которые я чаще всего использую в качестве источников цистеина. В качестве важной добавки с точки зрения поддержания уровня глутамина и глицина я рекомендую варенный в течение пяти или шести часов бульон на бараньих или телячьих костях животных известного происхождения, а также порошкообразные желатиновые добавки, если потребление белка недостаточно. Пока обсуждается вопрос о повышении уровня гистамина и глутаминовой кислоты при длительном приготовлении костного бульона, я легко могу сказать по своему клиническому опыту, что потребление костного бульона в течение суток снизило уровень тревожности у большинства моих пациентов. Костный бульон включен в программу питания, которую мы рекомендуем уже много лет. Помимо добавок, которые будут поддерживать индивидуальный цикл метилирования, большое значение при необходимости имеют добавки селена, витаминов С и Е. Если добавки витамина Е доступны в гамма-формах и смешанных/токофероловых формах, их можно использовать более эффективно с клеточной точки зрения.
Мелатонин – одно из основных веществ, обеспечивающих поддержку функций глутатиона. Не думайте, что мелатонин – это добавка, которая используется только для того, чтобы лучше засыпать. О мелатонине можно сказать куда больше. Мелатонин участвует в
• регуляции циркадного ритма (для решения проблем со сном);
• снижении интенсивности всех хронических болей, включая нейропатические;
• повышении качества жизни при депрессии;
• уменьшении окислительного повреждения;
• обладает противовоспалительной активностью за счет подавления (ингибирования) синтеза 5-LOX и COX-2;
• поддержании циркадного ритма кишечником днем и мозгом ночью;
• заживлении поврежденных тканей.
Мелатонин синтезируется из аминокислоты триптофана, которую вы получаете из куриного мяса, рыбы и шпината, при наличии достаточного количества желудочной кислоты и пищеварительных ферментов. В присутствии триптофана, железа, фолиевой кислоты, витамина D, магния, цинка, витаминов С, В6, В3 выделяется серотонин, а серотонин превращается в мелатонин посредством реакции метилирования.
Место его выработки в мозге – шишковидная железа, хотя в кишечнике его гораздо больше, чем в шишковидной железе и кровотоке. Ночью, в темноте, мозг становится главным производственным центром.
Синий свет из-за длины волны негативно влияет на синтез мелатонина. Обычно этот процесс начинается в одиннадцать часов вечера и достигает наивысшего уровня к двум часам ночи.
“Рецепторы мелатонина имеются в головном мозге, сетчатке глаза, сердечно-сосудистой системе, печени, желчном пузыре, кишечнике, почках, иммунных клетках, жировых клетках, эпителиальных клетках простаты и молочной железы, гранулезных клетках яичников, мышечных клетках матки и коже. Короче говоря, в организме нет места, где не действовал бы мелатонин”.
Наверное, лучший способ поддерживать в норме мелатонин в организме – соблюдать режим, вовремя ложиться спать, обеспечивая регулярный сон, здоровое функционирование пищеварительной системы и баланс метилирования. Поддержка мелатонином занимает важное место в моей клинической практике. Хотя есть данные, что добавки мелатонина подавляют вырабатываемый нами мелатонин (преобладающая теория – светочувствительность в супрахиазматическом ядре), если нет особых условий (риск рака молочной железы, перенесенный рак молочной железы, высокий окислительный стресс, аутоиммунные заболевания, некоторые проблемы с пищеварительной системой), я все равно обычно рекомендую принимать препарат замедленного действия в дозе около 5 мг в течение нескольких месяцев.
Витамины и минералы, связанные с метилированием
Форма B12, участвующая в метилировании, – это метилкобаламин. Поскольку метилкобаламин пока нельзя измерить непосредственно при обследованиях, мы можем видеть только общий уровень B12. Очевидно, значения, которые обычно приводятся в качестве нормальных (например, 200–1100 пг/мл) при обследованиях, слишком широкие. B12 следует оценивать в комплексе с результатами всех тестов, упомянутых в этом разделе, а также очень важно посмотреть значения гомоцистеина. Мы стремимся к таким показателям B12 и фолиевой кислоты, которые обеспечат желаемое значение гомоцистеина в диапазоне 6–8 мкмоль/л (согласно моему клиническому опыту, B12 обычно превышает 600 пг/мл). К сожалению, не припомню, чтобы при приеме добавок B12 в несколько микрограммов в день (RDA) у моего пациента повышался уровень B12 или снижался уровень гомо-цистеина.
“Если у человека с высоким уровнем гомоцистеина уровень B12 составляет 100–200 пг/мл, основной целью становится пополнение запасов B12, а затем при необходимости прием добавок метилфолата. При дефиците метилкобаламина формы фолата не участвуют в цикле метилирования”.
Если метилкобаламин назначить непосредственно при дефиците B12 человеку с интенсивным воспалением, повышенной кишечной проницаемостью, резистентностью к инсулину и потребностью в глутатионе, у него могут возникнуть побочные эффекты: повышенная тревожность, постназальный затек, боли в суставах, мышечные боли, чувствительность к метилу. По таким вопросам лучше всегда консультироваться с врачом.
Идеальная форма В12 для восполнения его запасов – гидроксикобаламин. Для людей с хроническими заболеваниями, такими как желудочно-кишечные проблемы, в частности, атрофический гастрит, внутримышечное введение гидроксикобаламина будет гораздо более эффективным. Мясо, печень и рыба богаты B12. Ну, а если вы уверены, что все реакции, которые будут происходить до тех пор, пока фолиевая кислота не превратится в метилфолат, будут протекать нормально, вы можете использовать эту синтетическую добавку. Поскольку меня самого это не очень устраивает, я предпочитаю регулярно употреблять зеленые листовые овощи (воздействие токсинов минимально, если вы берете овощи у проверенного производителя. Если вы не уверены в качестве, то после мытья овощей их можно замочить в газированной воде в течение как минимум десяти минут, а затем в уксусе, тоже на десять минут. Первый процесс поможет удалить остатки пестицидов на поверхности, хотя бы частично).
Если бы нужно было прописать фолиевую кислоту людям с высоким уровнем гомоцистеина и, что наиболее важно, нарушениями в гене MTHFR, я бы прежде всего предложил добавление фолиевой кислоты в форме метилфолата после восполнения запасов B12. Возможно, по мере того как эта проблема станет более известной, распространение получат такие формы, как фолиевая кислота и комбинация фолиевой кислоты и метилфолата.
Магний – один из жизненно важных минералов на клеточном уровне. Он присутствует в каждой точке выработки энергии. Образование основного метильного переносчика SAMe, одной из важнейших реакций метилирования, облегчает вместе с АТФ именно магний. При его дефиците могут наблюдаться тревога, нервозность, чувство подавленности, гиперактивность, бессонница, напряжение, снижение чувствительности к инсулину, проблемы с сердечным ритмом, утренняя усталость, запоры, судороги, остеопороз, ПМС, приступы гнева.
“Первое, что должно приходить на ум при виде взрослого или ребенка с диагнозом гиперактивности, – дефицит магния (наряду с железом). В двух различных исследованиях, проведенных на детях, было показано, что комбинация магния и витамина B6 снижает возбудимость центральной нервной системы и уменьшает поведенческие проблемы, как и ожидалось”.
Выявить дефицит магния при рутинных обследованиях очень сложно, поскольку большая его часть пребывает внутри клеток и в костях, в крови его менее 1 %. Представьте себе друга, с которым вы чувствуете себя наиболее комфортно, уютно и спокойно (вам повезло, если он есть), – это ваш магний. Точно так же клетка чувствует себя, когда в ней он есть. Я не сомневаюсь, что в ближайшие годы станут доступны тесты, которые помогут надежно отслеживать уровень магния, но, по крайней мере, на данный момент проверка уровня внутриэритроцитарного магния кажется гораздо более надежным способом с точки зрения точности данных.
Я провожу внутриэритроцитарный тест на магний большинству своих пациентов в течение длительного времени и слежу за изменениями уровня после приема добавок магния, которые прописываю. Бананы, авокадо, миндаль и шпинат – важные источники магния. Мы понимаем, что выявить дефицит магния с помощью классических тестов сложно. Допустим, мы клинически подозреваем дефицит магния, но на этот раз сталкиваемся со второй проблемой: какую форму препарата выбрать при дефиците магния?
Прежде чем планировать прием добавок магния, ваш врач проверит, здоровы ли функции ваших почек. Когда вы доберетесь до ближайшей аптеки, куда пойдете по рекомендации врача, то, скорее всего, столкнетесь с оксидом магния. Если наша цель – найти дополнительную поддержку при запорах, мы на правильном пути. Но когда нам нужна активность на клеточном уровне, предпочтительны более тонкие варианты. Еще два года назад в нашей стране[38] было очень сложно найти другую форму магния. Но теперь пациенты, за которыми я наблюдаю за рубежом, получают необходимые комбинации форм магния только из нашей страны, и это меня радует.
Планируя прием добавок магния, необходимо убедиться, что почки функционируют правильно. Еще один важный момент – следить за балансом магния и кальция. Прием магния может снизить уровень кальция. Если мы почитаем списки ожидания побочных эффектов от разных форм магния, увидим, что магний, полученный путем хелирования аминокислот, чрезвычайно функционален, особенно при использовании в эффективных дозах.
“Подводя итог, можно сказать, что глицинат и таурат магния кажутся эффективными формами при жалобах на тревогу, беспокойство и бессонницу, манат магния – при фибромиалгии, мигрени и хронической боли, а цитрат магния – при запорах, наличии камней из оксалатов кальция в почках, судорогах и нарушениях сердечного ритма”.
Уверен, что после прочтения этой книги цинк будет значить для вас гораздо больше, чем просто минерал, добавляемый в шампуни от выпадения волос. Цинк способствует здоровому функционированию фермента метионинсинтазы в цикле метилирования. Он действует как катализатор для более чем трехсот процессов, таких как синтез углеводов, жиров, белков, нуклеиновых кислот, метаболизм. Цинк участвует в формировании вкуса и запаха, работе иммунной системы, особенно функций Т-лимфоцитов и NK-клеток. Он также играет большую роль в заживлении ран, вызванных язвами и диабетом. Должен добавить, что это минерал, который я всегда имею при себе во время гриппа.
У человека с дефицитом цинка, скорее всего, будет депрессия, незаживающие раны, недостаток энергии, диарея и слабая иммунная система. При дефиците цинка функции металлотионеина нарушаются и повышается восприимчивость к окислительному повреждению. Устрицы, сырые тыквенные семечки, семена подсолнечника, миндаль, говядина и бобовые являются важными источниками цинка. Безопасный диапазон содержания цинка в крови, который не вызывает беспокойства, составляет 100–110 мкг/дл.
Низкое значение щелочной фосфатазы (оптимальный диапазон 70–90 МЕ/л), выявленное в анализах крови, может быть значимым показателем дефицита цинка.
“Если мы хотим принимать цинк в виде добавки, самой идеальной формой будет пиколинат. В нормальных условиях наша ежедневная потребность в цинке составляет около 10‒15 мг. Добавки цинка могут вызвать дефицит меди, поэтому рекомендую добавить к цинку одну десятую часть меди (предпочтительны формы пиколината, глицината или глюконата)”.
Потребность в цинке может увеличиваться у курильщиков (токсичность кадмия), людей с высокой окислительной нагрузкой и воспалением, нарушениями кишечного всасывания и недостаточным питанием.
Витамин В2 – очень важный элемент, о котором нечасто упоминают в анализах, находящийся в центре цикла метилирования. Это основное «топливо» гена MTHFR.
Неудивительно, что одно исследование пришло к выводу, что после введения B2 людям с гомозиготным наследственным заболеванием MTHFR C677T снижался уровень артериального давления.
“На самом деле это означает следующее: даже если ген унаследован с дефектом, когда вы обеспечите его питательными веществами и максимизируете рабочий потенциал, существующий дефект может не проявиться”.
Поэтому в случае повышения уровня гомоцистеина одним из самых важных помощников для нас становится витамин B2. Нужно помнить, что витамин B2 помогает главному окисленному антиоксиданту глутатиону восстановить функциональность. Своим пациентам я уже много лет рекомендую не B2, а его активную форму R5P (рибоза-5-фосфат). Здоровое функционирование фермента MTHFR чрезвычайно важно для метилирования и цикла фолиевой кислоты. В этой реакции участвует как раз активная форма R5P, а не непосредственно B2 (для преобразования которого в R5P необходимы цинк и гормон T4). Все в системе взаимосвязано. У человека, ведущего здоровый образ жизни и регулярно употребляющего печень, вряд ли возникнет дефицит витамина B2. Кроме того, очень ценными источниками витамина B2 являются субпродукты, такие как почки и сердце, а также миндаль.
Цистатионинбета-синтаза (CBS) – это фермент, необходимый для пути № 3, пути транссульфации, – одного из тех, что обеспечивают образование гомоцистеина, конечного продукта цикла метилирования. Витамин B6 чрезвычайно важен для здорового функционирования CBS. Как известно, этот путь обеспечивает выработку очень важных для организма молекул, таких как глутатион и таурин. Любой механизм, который потенциально нарушает образование глутатиона, может привести к увеличению содержания перекиси водорода, окислительному стрессу и блокировке реакций метилирования. Все эти системы переплетены друг с другом и не так просты, как их можно изобразить стрелками, которые мы рисуем на биохимических схемах.
Первое, что приходит на ум при упоминании витамина В6, – его вклад в образование нейромедиаторов, таких как серотонин, дофамин и гамма-аминомасляная кислота. Другими словами, он эффективен при работе с различными клиническими состояниями: от депрессивного настроения до тревоги, от проблем с вниманием до гиперактивности и даже эпилептических припадков. Несмотря на то что витамин B6 не входит в число параметров, на которые мы обращаем внимание при рутинных анализах крови, это, очевидно, очень важный элемент биохимических процессов. Информацию об уровне витамина B6 и его функциональном состоянии можно извлечь из значения АЛТ (аланинаминотрансферазы), которое измеряется для оценки наличия повреждения или разрушения печени на клеточном уровне.
“Если уровень АЛТ в анализах крови ниже 12, нужно задуматься о дефиците витамина B6. Уровень пири-доксальфосфата в плазме ниже 30 нмоль/л или высокий уровень ксантурината и киенурината в тесте на органическую кислоту мочи – также важные индикаторы дефицита витамина B6”.
Как мы уже упоминали, говоря о других витаминах группы B, активной функциональной формой витамина B6 является P5P (пиридоксаль-5-фосфат). Чтобы B6 превратился в P5P, в организме нужен магний. Таким образом, неактивный витамин B6 может оказаться недостаточно эффективным при дефиците магния, что мы и наблюдаем очень часто. Я рекомендую добавки B6 в форме P5P всем своим клиентам, которым я планирую вводить витамин В6.
Триметилглицин, или бетаин, – это важный поддерживающий элемент пути цикла метилирования № 2, который вступает в игру, когда путь № 1 блокируется, например, из-за дефицита витамина B12 или 5-MTHF. Его наиболее важным источником является красная свекла, и его также можно синтезировать из холина.
Тот факт, что он синтезируется из холина, может вызвать дефицит холина в тех случаях, когда путь номер один не используется активно. Я рекомендую некоторым своим пациентам с высоким уровнем гомоцистеина регулярно употреблять сок красной свеклы (TMG) и печень (холин) в дополнение к другим добавкам.
Иногда также могу порекомендовать 1000–1500 мг три-метилглицина в день некоторым из них, у которых нет чувствительности к метилу, для поддержания цикла метилирования, если это необходимо.
Витамин D играет важную роль, особенно в определении того, какая область метильных групп ДНК будет добавлена или удалена на уровне генов. Он чрезвычайно важен для многих функций наших клеток. Из-за рахита, возникающего в результате его дефицита, знания о его значении прежде ограничивались только костями. Витамин D – это балансир иммунной системы, он также играет важную роль в регулировании артериального давления и защите от многих видов рака. Если вы хотите защитить себя от заболеваний центральной нервной системы или депрессии, я рекомендую вам не лишать себя витамина D.
Убеждение, что можно поддерживать необходимый уровень витамина D от солнца, разочаровывают как с точки зрения науки, так и опыта. Чтобы обеспечить этот синтез, нужно загорать в течение примерно двадцати минут без солнцезащитных очков и без защитного крема, что может быть и эффективно, но довольно вредно, особенно в летние месяцы, когда уровень UVA-лучей наиболее высок.
“С точки зрения синтеза витамина D воздействие UVA-лучей при длительном загаре, темная кожа, использование солнцезащитного крема и принятие душа сразу после принятия солнечных ванн – негативные факторы”.
В анализах крови оптимальным считается диапазон витамина D 60–80 нг/мл. У значительной части общества наблюдается серьезный дефицит витамина D, и компенсировать этот дефицит без дополнительной поддержки очень сложно. Прием витамина D из расчета одна тысяча единиц на десять килограммов веса в день как альтернатива очень высоким дозам в триста тысяч единиц в ампулах, рекомендуемым для употребления, или очень низким ежедневным дозам в четыреста-тысячи единиц, приводит к благоприятным изменениям у большинства моих пациентов в течение нескольких месяцев. Принимая витамин D при поддержке врача, следует соблюдать осторожность в отношении повышения уровня кальция и подавления паратгормона.

Рис. 17. Витамин D
Еще один важный момент – обеспечить, чтобы кальций, всасывание которого в кишечнике может увеличиться, направлялся в кости при поддержке витамина D. Эту роль выполняет витамин К2. Витамин К2 обычно используют наряду с витамином D. Для эффективного функционирования витамину D необходим достаточный уровень магния.
 ТЕЛЕГРАМ
ТЕЛЕГРАМ Книжный Вестник
Книжный Вестник Поиск книг
Поиск книг Любовные романы
Любовные романы Саморазвитие
Саморазвитие Детективы
Детективы Фантастика
Фантастика Классика
Классика ВКОНТАКТЕ
ВКОНТАКТЕ